题目内容
(1)25℃时,0.05 mol/L H2SO4溶液的pH=________;0.05 mol/L Ba(OH)2溶液中c(H+)=________.
(2)某温度下纯水中的c(H+)=2.0×10-7 mol/L,则此时溶液中的c(OH-)=________;若温度不变,滴入稀盐酸,使c(H+)=5.0×10-4 mol/L,则溶液中c(OH-)=________,此时溶液中由水电离产生的c(H+)=________.
答案:
解析:
解析:
答案:
(1)1 1.0×10-13 mol/L(2)2.0×10-7 mol/L 8.0×10-11 mol/L 8.0×10-11 mol/L
讲析:


练习册系列答案
相关题目
(4分)化学上常用电离度表示电解质的相对强弱:α=已电离的电解质分子数/溶液中原有电解质的总分子数×100%。
|
物质(微粒)及编号 |
电离度α |
|
A.硫酸溶液(第一步完全电离): HSO |
10% |
|
B.硫酸氢钠溶液:HSO |
29% |
|
CH3COOH |
1.33% |
|
D.盐酸:HCl=H++Cl- |
100% |
(1)25℃时,0.1 mol·L-1上述几种溶液中,c(H+)从大到小的顺序是_____(填序号);
(2)25℃时,0.1 mol·L-1硫酸溶液中HSO的电离度小于相同温度下0.1 mol·L-1硫酸氢钠溶液中HSO的电离度,其原因是__________________。
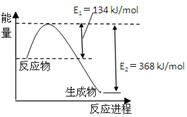
 N2(g)+2CO2(g)的△H是 。
N2(g)+2CO2(g)的△H是 。 H++SO
H++SO H++SO
H++SO COOH
COOH CH3COO-+H+
CH3COO-+H+