题目内容
8.一定温度下,对于可逆反应N2O4(g)?2NO2(g)△H>0,在密闭容器中达到平衡状态.下列有关说法中正确的是( )| A. | 保持温度不变,缩小容器的体积,平衡向逆反应方向移动,再次达到平衡时气体的颜色变浅了 | |
| B. | 若保持恒温恒压,再充入一定量的NO2气体,当容器的体积不再变化时表明重新达到平衡状态 | |
| C. | 保持容器的体积不变,升高温度,正反应速率加快,逆反应速率减慢,平衡向正反应方向移动 | |
| D. | 恒温恒容条件下,再充入一定量的N2O4,达到新平衡时NO2的体积分数比原平衡的大 |
分析 A、缩小体积,各种物质的浓度均增大,所以颜色加深;
B、加入少许NO2平衡向逆反应方向移动,N2O4浓度增大,正反应速率增大,逆反应速率瞬间增大,然后降低;
C、升高温度,正逆反应速率均加快;
D、体积不变,加入少许N2O4,平衡向正反应移动,NO2浓度增大,NO2是红棕色气体.
解答 解:A、缩小体积,各种物质的浓度均增大,所以颜色加深,故A错误;
B、少许NO2平衡向逆反应方向移动,N2O4浓度增大,正反应速率增大,逆反应速率瞬间增大,然后降低,当容器的体积不再变化时表明重新达到平衡状态,故B正确;
C、升高温度,正逆反应速率均加快,故C错误;
D、恒温恒容,再充入一定量的四氧化二氮,相当于加压效果,所以达到新平衡时二氧化氮的体积分数比原平衡的小,故D错误,
故选B.
点评 本题主要考查的是化学反应平衡的影响因素,涉及压强、浓度、温度等的影响,难度不大.

练习册系列答案
相关题目
18.用酸性氢氧燃料电池(甲池)为电源进行电解的实验装置(乙池,一定条件下可实现有机物的电化学储氢)如图所示.甲池中C为含苯的物质的量分数为10%的混合气体,D为l0mol混合气体其中苯的物质的量分数为24%(杂质不参与反应),E为标准状况下2.8mol气体(忽略水蒸汽),下列说法正确的是( )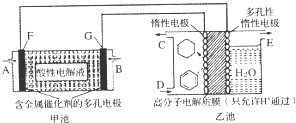

| A. | 甲池中A处通入H2,E处有O2放出 | B. | 甲池中H+由F极移向G极 | ||
| C. | 乙池中阴极区只有苯被还原 | D. | 导线中共传导11.2mol电子 |
16.已知W、X、Y、Z为原子序数依次增大的短周期主族元素,X、Y、Z同周期,W、Z同主族,其中X、Y为金属元素,W与Y的原子序数相差5,下列说法正确的是( )
| A. | X离子的氧化性大于Y离子 | B. | W的气态氢化物的稳定性比Z的弱 | ||
| C. | 含Y的盐溶液一定显酸性 | D. | X离子的半径小于W离子 |
3.只用一种试剂即可鉴别乙醇、乙醛、乙酸、甲酸等有机物的溶液,这种试剂是( )
| A. | 新制生石灰 | B. | 新制氢氧化铜 | C. | 浓溴水 | D. | 银氨溶液 |
2.浓硫酸是一种重要的化工产品.某化学兴趣小组拟探究Cu与浓H2SO4的反应.
Ⅰ.[查阅资料]
铜与浓硫酸反应产生黑色物质的相关性质资料如下表:
Ⅱ.[探究过程]

(1)试管A中发生的反应的主要化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
(2)反应进行一段时间可观察到试管B中的现象为溶液由红色变成无色.
(3)试管C浸有NaOH溶液的棉团与试管E的NaOH溶液的作用是否相同相同(填“相同或不相同”)
(4)如同时将试管B换成试管D,将试管C换成试管E,并从试管D的直立导管中通入另一种气体,试管D中产生白色沉淀,则气体可以是NH3(NO2或ClO2)、Cl2(O3或O2或Br2蒸汽)(填一种化合物和一种单质的化学式);试管E中CCl4的作用是防倒吸.
(5)用简单方法证明A试管中反应所得产物含有铜离子的操作方法是(停止反应,冷却后),取A中溶液少许于一盛有少量水的烧杯(试管)里,摇匀,观察溶液颜色呈蓝色;分离出试管E中的上层液体,其分离的操作名称为分液.
Ⅲ.[问题反思]
(6)仅由上述资料及探究过程可得出的正确结论是abd.
a.铜与浓硫酸作用所涉及的反应可能不止一个
b.硫酸浓度选择适当,可避免产物中出现黑色物质
c.反应发生条件之一是硫酸浓度≥15mol/L
d.硫酸浓度越大,黑色物质越快出现,越难消失.
Ⅰ.[查阅资料]
铜与浓硫酸反应产生黑色物质的相关性质资料如下表:
| 资料1 | 硫酸浓度mol/L | 黑色物质出现的温度∕℃ | 黑色物质消失的温度∕℃ |
| 15 | 约150 | 约236 | |
| 16 | 约140 | 约250 | |
| 18 | 约120 | 不消失 | |
| 资料2 | X射线衍射晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种. | ||

(1)试管A中发生的反应的主要化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
(2)反应进行一段时间可观察到试管B中的现象为溶液由红色变成无色.
(3)试管C浸有NaOH溶液的棉团与试管E的NaOH溶液的作用是否相同相同(填“相同或不相同”)
(4)如同时将试管B换成试管D,将试管C换成试管E,并从试管D的直立导管中通入另一种气体,试管D中产生白色沉淀,则气体可以是NH3(NO2或ClO2)、Cl2(O3或O2或Br2蒸汽)(填一种化合物和一种单质的化学式);试管E中CCl4的作用是防倒吸.
(5)用简单方法证明A试管中反应所得产物含有铜离子的操作方法是(停止反应,冷却后),取A中溶液少许于一盛有少量水的烧杯(试管)里,摇匀,观察溶液颜色呈蓝色;分离出试管E中的上层液体,其分离的操作名称为分液.
Ⅲ.[问题反思]
(6)仅由上述资料及探究过程可得出的正确结论是abd.
a.铜与浓硫酸作用所涉及的反应可能不止一个
b.硫酸浓度选择适当,可避免产物中出现黑色物质
c.反应发生条件之一是硫酸浓度≥15mol/L
d.硫酸浓度越大,黑色物质越快出现,越难消失.
3.已知:①1mol H2 分子中化学键断裂时需要吸收 436kJ 的能量 ②1mol Cl2 分子中化学键断裂时需要吸收 243kJ 的能量 ③由H原子和Cl原子形成1mol HCl分子时释放 431kJ 的能量,则下列叙述正确的是( )
| A. | 氢气和氯气反应生成氯化氢气体的热化学方程式是 H2 (g)+Cl2 (g)═2HCl(g) | |
| B. | 氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H═+183 kJ•mol-1 | |
| C. | 氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H═-183 kJ•mol-1 | |
| D. | 氢气和氯气反应生成 1 mol 氯化氢气体,反应的△H═-183 kJ•mol-1 |

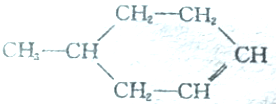 可以写成
可以写成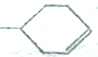 ,现有有机物A,可写为
,现有有机物A,可写为