题目内容
下列有机物中不溶于水且比水轻的是( )
| A、CCl4 |
| B、乙酸 |
| C、苯 |
| D、溴苯 |
考点:卤代烃简介,苯的性质
专题:有机化学基础
分析:烃、卤代烃等难溶于水,羧酸、醇等一般易溶于水,结合常见有机物的密度分析.
解答:
解:乙酸与水互溶;CCl4、苯、溴苯都难溶于水,CCl4和溴苯的密度大于水,苯的密度小于水,所以不溶于水且比水轻的是苯,
故选C.
故选C.
点评:本题考查了有机物的溶解性和密度,侧重于基础知识的考查,题目难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
为探究锌与稀盐酸反应速率[以v(H2)表示],向反应混合液中加入某些物质,下列判断正确的是( )
| A、加入铜粉,v(H2)增大 |
| B、加入NaCl固体,会增大Cl-浓度,从而使v(H2)增大 |
| C、加入NaHSO4固体v(H2)不变 |
| D、加入水,锌不与水反应,v(H2)不变 |
下列化学反应中,属于氧化还原的化合反应是( )
| A、Na2CO3+CaCl2═CaCO3↓+2NaCl | ||||
| B、Fe+CuSO4═Cu+FeSO4 | ||||
C、2NaHCO3
| ||||
| D、Na2O2+SO2═Na2SO4 |
已知:断开1molN≡N需要吸收akJ热量,断开1molH-H需要吸收bkJ热量,断开1molN-H需要吸收ckJ热量.向某密闭容器中通入1molN2和3molH2,在一定条件下发生反应:N2(g)+3H2(g)?2NH3(g)(放热反应).下列描述中正确的是( )
| A、N2和H2具有的总能量一定比NH3具有的总能量低 |
| B、a、b、c三者的关系为:a+3b<2c |
| C、向密闭容器中通入1mol N2和3mol H2,反应放出的热量必为(6c-a-3b)kJ |
| D、形成1mol N-H会放出c kJ热量 |
将镁带投入盛放在敞口容器内的盐酸里,反应速率用产生的氢气的速率表示,在下列因素中:
①盐酸的浓度,
②镁带的表面积,
③溶液的温度,
④盐酸的体积,
⑤氯离子的浓度,
其中影响反应速率的因素是( )
①盐酸的浓度,
②镁带的表面积,
③溶液的温度,
④盐酸的体积,
⑤氯离子的浓度,
其中影响反应速率的因素是( )
| A、①④ | B、③⑤ |
| C、①②③⑤ | D、①②③ |
下列化学用语说法正确的是( )
A、甲基的电子式: | ||
B、乙烯的比例模型: | ||
C、质子数为53,中子数为78的碘原子:
| ||
| D、次氯酸的结构式:H─O─Cl |
与图中相对应的叙述是( )
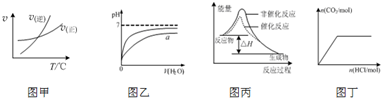

| A、由图甲表示的反应速率随温度变化的关系可知该反应的△H>0 |
| B、图乙表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是醋酸 |
| C、图丙表示该反应为放热反应,且催化剂能改变反应的焓变 |
| D、图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系 |
NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,11.2L的戊烷所含的分子数为0.5NA |
| B、28g乙烯所含共用电子对数目为4NA |
| C、1mol甲基的电子数目为7NA |
| D、现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
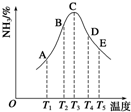 在容积相同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2(g)+3H2(g)?2NH3(g),并分别在t秒时测定其中NH3的体积分数,如图:
在容积相同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2(g)+3H2(g)?2NH3(g),并分别在t秒时测定其中NH3的体积分数,如图: