题目内容
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、80 g硝酸铵(NH4NO3)中含有的氮原子数是NA |
| B、在常温常压下,71 g Cl2含有的分子数为0.5NA |
| C、16 g氧气和16 g臭氧所含有的原子数均为NA |
| D、2 mol金属铝与足量的盐酸反应,共失去4NA个电子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.1mol硝酸铵中含有2mol氮原子;
B.71 g Cl2的物质的量是1mol;
C.质量相同的单质所含氧元素质量相等;
D.依据铝的原子结构最外层电子为3,全部反应时依据反应的铝计算失去电子数.
B.71 g Cl2的物质的量是1mol;
C.质量相同的单质所含氧元素质量相等;
D.依据铝的原子结构最外层电子为3,全部反应时依据反应的铝计算失去电子数.
解答:
解:A.80 g硝酸铵(NH4NO3)的物质的量是1mol,含有的氮原子数是2NA,故A错误;
B.71 g Cl2的物质的量是1mol,含有的分子数为NA,故B错误;
C.氧气和臭氧都是氧元素组成的单质,质量相同的单质所含氧元素质量相等;16 g氧气和16 g臭氧所含的原子数相等均为NA,故C正确;
D.铝的原子结构最外层电子为3,2mol金属铝与足量的盐酸反应,共失去了6NA个电子,故D错误.
故选C.
B.71 g Cl2的物质的量是1mol,含有的分子数为NA,故B错误;
C.氧气和臭氧都是氧元素组成的单质,质量相同的单质所含氧元素质量相等;16 g氧气和16 g臭氧所含的原子数相等均为NA,故C正确;
D.铝的原子结构最外层电子为3,2mol金属铝与足量的盐酸反应,共失去了6NA个电子,故D错误.
故选C.
点评:本题考查了阿伏伽德罗常数的应用,主要考查了质量换算物质的量计算微粒数,原子结构的分析和氧化还原反应的电子转移计算,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
青霉素V钾的化学结构式为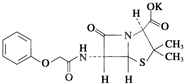 下列有关说法错误的是( )
下列有关说法错误的是( )
 下列有关说法错误的是( )
下列有关说法错误的是( )| A、青霉素V钾为芳香族化合物 |
| B、青霉素V钾的分子式为C16H17KN2O5 |
| C、青霉素V钾在酸性条件下最终生成青霉氨基酸 |
| D、使用本品前需先进行青霉素皮肤敏感试验 |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4L SO3中所含有分子数为NA |
| B、常温下,28 g 乙烯和丙烯的混合物中所含化学键一定为6NA |
| C、在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定为4NA |
| D、1 L 1mol/L NH4NO3溶液中氮原子数目小于2NA |
下列有关试剂的保存方法错误的是( )
| A、少量的钠保存在煤油中 |
| B、新制的氯水保存在棕色试剂瓶中 |
| C、漂白粉要密闭保存 |
| D、浓盐酸保存在敞口试剂瓶中即可 |
下列物质能使干燥的蓝色石蕊试纸先变红又褪色的是( )
| A、久置的氯水 |
| B、氯气溶于无水酒精所形成的溶液 |
| C、盐酸 |
| D、盐酸酸化的漂白粉溶液 |
下列表达式正确的是( )
A、O2-的结构示意图: | ||
B、碳原子的L层电子轨道表示式: | ||
| C、硫离子的核外电子排布式:1s22s22p63s23p4 | ||
D、碳-12原子:
|
 已知水是人体的重要组成部分,是人体中含量最多的一种物质,而“四种基本反应类型与氧化还原反应的关系”可用如图表达:
已知水是人体的重要组成部分,是人体中含量最多的一种物质,而“四种基本反应类型与氧化还原反应的关系”可用如图表达: