题目内容
11.1mol CO(NH2)2中含1mol碳原子,2mol氮原子,4mol氢原子,1 mol氧原子.分析 CO(NH2)2分子含有1个C原子、2个N原子、4个H原子、1个O原子,故含有碳原子、氧原子的物质的量等于CO(NH2)2的物质的量,N原子物质的量为CO(NH2)2的2倍,H原子物质的量为CO(NH2)2的4倍,由此分析解答.
解答 解:CO(NH2)2分子含有1个C原子、2个N原子、4个H原子、1个O原子,则:n(C)=n[CO(NH2)2]=1mol,n(N)=2n[CO(NH2)2]=2mol,n(H)=4n[CO(NH2)2]=4mol,n(O)=n[CO(NH2)2]=1mol,水分子含有1个氧原子,二者含有氧原子数目相等,则二者物质的量相等,水的物质的量为1mol,故答案为:1;2;4;1.
点评 本题考查物质的量有关计算,比较基础,注意对化学式意义的理解.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列反应完毕后有沉淀的是( )
| A. | KOH 溶液与FeCl3 溶液加足量稀硝酸 | |
| B. | Ba(OH)2 溶液与KNO3溶液加足量H2SO4 | |
| C. | CuSO4溶液与NaOH 溶液加足量稀盐酸 | |
| D. | BaCl2 溶液与Na2CO3 溶液加足量稀醋酸 |
19.下列参数比较及解释均正确的是( )
| 选项 | 参数 | 比较 | 解释 |
| A | 还原性 | Br->Cl- | 元素的非金属性越强,简单阴离子的还原性越弱 |
| B | 半径 | Na+<Mg2+<Al3+ | 同一周期粒子半径随原子序数的递增逐渐减小 |
| C | 酸性 | H2SO3>H2CO3 | 元素的非金属性越强,其含氧酸的酸性越强 |
| D | 沸点 | HF<HCl<HI | 组成结构相似的物质,相对分子质量越大沸点越高 |
| A. | A | B. | B | C. | C | D. | D |
6.碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
(1)真空碳热还原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
2Al2O3(s)+2AlCl3(g)+6C(s)═6AlCl(g)+6CO(g)△H=akJ•mol-1
3AlCl(g)═2Al(l)+AlCl3(g)△H=bkJ•mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=(0.5a+b)kJ•mol-1(用含a、b的代数式表示);
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H=QkJ•mol-1.在T1℃时,反应进行到不同时间测得各物质的浓度如下:
①0~10min内,NO的平均反应速率v(NO)=0.032 mol•L-1•min-1,T1℃时,该反应的平衡常数K=0.25;
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是ad(填字母编号).
a.通入一定量的NO
b.加入一定量的活性炭
c.加入合适的催化剂
d.适当缩小容器的体积
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q<0(填“>”或“<”).
④在绝热恒容条件下,能判断该反应一定达到化学平衡状态的依据是bcd(填选项编号).
a.单位时间内生成2nmol NO(g)的同时消耗nmol CO2(g)
b.反应体系的温度不再发生改变
c.混合气体的密度不再发生改变
d.反应体系的压强不再发生改变.
(1)真空碳热还原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
2Al2O3(s)+2AlCl3(g)+6C(s)═6AlCl(g)+6CO(g)△H=akJ•mol-1
3AlCl(g)═2Al(l)+AlCl3(g)△H=bkJ•mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=(0.5a+b)kJ•mol-1(用含a、b的代数式表示);
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H=QkJ•mol-1.在T1℃时,反应进行到不同时间测得各物质的浓度如下:
| 时间(min) 浓度(mol•L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是ad(填字母编号).
a.通入一定量的NO
b.加入一定量的活性炭
c.加入合适的催化剂
d.适当缩小容器的体积
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q<0(填“>”或“<”).
④在绝热恒容条件下,能判断该反应一定达到化学平衡状态的依据是bcd(填选项编号).
a.单位时间内生成2nmol NO(g)的同时消耗nmol CO2(g)
b.反应体系的温度不再发生改变
c.混合气体的密度不再发生改变
d.反应体系的压强不再发生改变.
16.在标准状况下①6.72L CH4 ②3.01×1023个HCl分子 ③3.4g NH3,这三种气体中氢原子个数从多到少的顺序表达正确的是( )
| A. | ①②③ | B. | ②③① | C. | ②①③ | D. | ①③② |
3.若要除去下列溶液中的杂质(括号内为杂质),请将选用的试剂及有关反应的化学方程式填入下表的空白处:
| 物质(杂质) | 试剂 | 有关化学方程式 |
| NaHCO3(Na2CO3) | CO2 | Na2CO3+H2O+CO2=2NaHCO3 |
| FeCl2(FeCl3) | Fe | 2FeCl3+Fe═3FeCl2 |
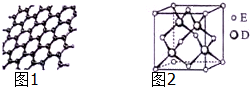 原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:
原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题: