题目内容
12. A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,它们之间的转化关系如图所示((图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).
A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,它们之间的转化关系如图所示((图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).回答下列问题:
(1)A的化学式为CO,D→C的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)若E和F均由两种元素组成,E的化学式为CH4或HCl;
(3)若E和F均由三种元素组成,写出指定的转化反应的化学方程式:
F→B+CH2SO4+Na2CO3=Na2SO4+H2O+CO2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑.
分析 A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,由转化可知A为CO、B为CO2,D为H2O2,C为H2O,若E和F均由两种元素组成,则E、F分别为CH4、HCl中的一种,若E和F均由三种元素组成,可以是碳酸钠与硫酸反应,也可以是碳酸钙与盐酸反应.
解答 解:A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,由转化可知A为CO、B为CO2,D为H2O2,C为H2O.
(1)A的化学式为CO,D→C的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,故答案为:CO;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)若E和F均由两种元素组成,则E、F分别为CH4、HCl中的一种,故答案为:CH4或HCl;
(3)若E和F均由三种元素组成,可以是碳酸钠与硫酸反应,也可以是碳酸钙与盐酸反应,F→B+C的反应方程式:H2SO4+Na2CO3=Na2SO4+H2O+CO2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑,
故答案为:H2SO4+Na2CO3=Na2SO4+H2O+CO2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评 本题考查无机物推断,属于猜测验证型,需要学生元素化合物知识,注意为初中常见物质之间的反应,难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
7.如图为镁元素的相关信息,由此不能得到的信息是( )


| A. | 镁属于金属元素 | |
| B. | 镁离子核内有12个质子 | |
| C. | 镁离子与硫离子的电子层数相等 | |
| D. | 在化学反应中,1个硫原子容易得到2个电子 |
4.图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)表中某元素最高正价氧化物的水化物与其氢化物之间能相互反应生成离子化合物,则该离子化合物的名称是硝酸铵,由元素④、⑥、⑦、⑧形成的简单离子的半径由大到小的顺序是Cl->O2->Na+>Al3= (用离子符号表示,下同).③、④、⑤元素的氢化物的沸点由高到低的顺序是H2O>HF>NH3.
(2)分别由上述两种元素组成、均为10e-的阴、阳离子,在加热条件下反应生成两种10e-的分子,写出该离子反应方程是NH4++OH-=NH3+H2O.
(3)由表中四种元素形成X、Y、Z、M、N等常见物质,X、Y含有一种相同元素,其中X焰色反应呈黄色,可发生以下反应:

①X、Y与水混合后反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓.
②N→⑦的单质反应的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
③若将Y溶液加热蒸干、灼烧后得到的物质的化学式是Al2O3.
 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | |||||
(2)分别由上述两种元素组成、均为10e-的阴、阳离子,在加热条件下反应生成两种10e-的分子,写出该离子反应方程是NH4++OH-=NH3+H2O.
(3)由表中四种元素形成X、Y、Z、M、N等常见物质,X、Y含有一种相同元素,其中X焰色反应呈黄色,可发生以下反应:

①X、Y与水混合后反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓.
②N→⑦的单质反应的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
③若将Y溶液加热蒸干、灼烧后得到的物质的化学式是Al2O3.
1.下列说法中正确的是( )
| A. | 苯使溴水层褪色属于加成反应 | |
| B. | 乙烯与水反应生成乙醇属于水解反应 | |
| C. | 同二甲苯只有一种结构说明苯分子中不存在单双链交替 | |
| D. | 等质量环丁烷(C4H8)和乙烯(C2H4)完全燃烧,消耗的氧气量相等 |
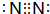 ,物质甲分子的结构式
,物质甲分子的结构式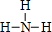 .
. .
. ;
; ,其核磁共振氢谱中有2个吸收峰.
,其核磁共振氢谱中有2个吸收峰.