题目内容
9.写出下列物质在水溶液中的电离方程式:①H2SO4:H2SO4═2H++SO42-; ②CaCl2:CaCl2=Ca2++2Cl-; ③KOH:KOH=K++OH-;④NaNO3:NaNO3═Na++NO3-.
分析 化学式和离子符号表示电离过程的式子,称为电离方程式,首先判断电解质的类型及电离出的阴阳离子,离子所带电荷数一般可根据它们在化合物中的化合价来判断,所有阳离子带的正电荷总数与所有阴离子所带的负电荷总数相等,离子团不能拆开,然后根据电解质的类型判断写可逆号还是等号,如果是多元弱酸,要分步电离,如果是多元弱碱,只需一步书写,最后要注意原子守恒、电荷守恒,据此即可解答.
解答 解:①硫酸电离时生成氢离子、硫酸根离子,其电离方程式为H2SO4═2H++SO42-,
故答案为:H2SO4═2H++SO42-;
②氯化钙为强电解质,完全电离,电离方程式为:CaCl2=Ca2++2Cl-,
故答案为:CaCl2=Ca2++2Cl-;
③氢氧化钾是强电解质,能完全电离,电离方程式为:KOH=K++OH-,
故答案为:KOH=K++OH-;
④硝酸钠是强电解质,在水溶液里完全电离生成钠离子和硝酸根离子,电离方程式为 NaNO3═Na++NO3-,
故答案为:NaNO3═Na++NO3-.
点评 本题考查电离方程式的书写,书写电离方程式时注意离子的正确书写、电荷守恒、离子团不能拆开,题目难度不大.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
19.V、W、X、Y是元素周期表中短周期元素,在周期表中的位置关系如图所示:
Z为第四周期常见元素,该元素是人体血液中血红蛋白的组成金属元素.V的最简单氢化物为甲,W的气态氢化物为乙,甲、乙混合时有白烟生成,甲能使湿润的红色石蕊试纸变蓝,W与Z可形成化合物ZW3.
下列判断正确的是( )
| Y | V | |||
| X | W |
下列判断正确的是( )
| A. | 原子半径:X>Y>V>W | |
| B. | X、W的质子数之和与最外层电子数之和的比值为 2:1 | |
| C. | 甲、乙混合时所生成的白烟为离子化合物,但其中含有共价键 | |
| D. | 在足量的沸水中滴入含有16.25 g ZW3的溶液可得到0.1 mol Z(OH)3 |
20.下列物质中属于纯净物的一组是( )
①冰水混合物 ②爆鸣气 ③铝热剂 ④普通玻璃 ⑤水玻璃 ⑥漂白粉 ⑦二甲苯 ⑧TNT
⑨溴苯 ⑩C5H10⑪含氧40%的氧化镁⑫花生油⑬福尔马林⑭密封保存的NO2气体.
①冰水混合物 ②爆鸣气 ③铝热剂 ④普通玻璃 ⑤水玻璃 ⑥漂白粉 ⑦二甲苯 ⑧TNT
⑨溴苯 ⑩C5H10⑪含氧40%的氧化镁⑫花生油⑬福尔马林⑭密封保存的NO2气体.
| A. | ①⑧⑨⑪ | B. | ②③④⑥ | C. | ⑦⑩⑫⑪⑭ | D. | ①④⑧⑨⑪⑫ |
4.下列现象与胶体的知识无关的是( )
| A. | 清晨,在茂密的树林中,可以看到从枝叶间透过的一道道光柱 | |
| B. | 工厂里用静电除尘 | |
| C. | 氨水和氯化铁溶液反应,生成氢氧化铁沉淀 | |
| D. | 不同品牌的墨水混用,导致钢笔出现堵塞 |
14.25℃时,下列说法正确的是( )
| A. | pH=2的醋酸溶液与pH=12的氢氧化钠溶液等体积混合,混合后溶液pH=7 | |
| B. | 将0.1mol•L-1氢氧化钠溶液与pH=1稀硫酸等体积混合,混合后的溶液pH<7 | |
| C. | 硫酸铵溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | pH相同的醋酸钠溶液、碳酸氢钠溶液、碳酸钠溶液,其物质的量浓度: c(CH3COONa)>c(NaHCO3)>c(Na2CO3) |
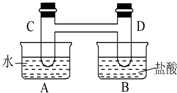 如图所示,在容器A中装有20℃的水50mL,容器B中装有1 mol/L的盐酸50mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:
如图所示,在容器A中装有20℃的水50mL,容器B中装有1 mol/L的盐酸50mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:
 已知常温下甲醛是一种无色、有刺激性气味的气体,易溶于水,是世界卫生组织(WHO)确认的致癌物和致畸物质之一.我国规定:居室中甲醛含量不得超过0.08mg/m3.可利用酸性高锰酸钾溶液测定甲醛含量.
已知常温下甲醛是一种无色、有刺激性气味的气体,易溶于水,是世界卫生组织(WHO)确认的致癌物和致畸物质之一.我国规定:居室中甲醛含量不得超过0.08mg/m3.可利用酸性高锰酸钾溶液测定甲醛含量. .
.