题目内容
1.氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2•6H2O的流程如图1: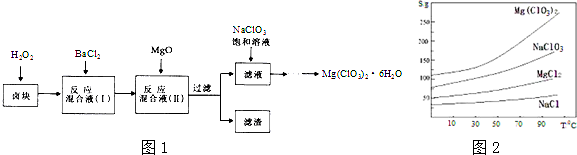
已知:①卤块主要成分为MgCl2•6H2O,含有MgSO4、FeCl2等杂质.
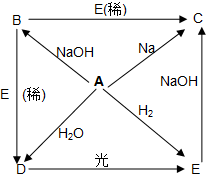
②四种化合物的溶解度(S)随温度(T)变化曲线如图2所示.回答下列问题:
(1)过滤时主要的玻璃仪器有漏斗、玻璃棒、烧杯
(2)加入BaCl2的目的是除去杂质离子,检验已沉淀完全的方法是静置,取上层清液适量于试管中,加入BaCl2溶液,若无白色沉淀生成,则SO42-沉淀完全
(3)加速卤块在H2O2溶液中溶解的措施有:将卤块粉碎或加热等 (写出一条即可)
(4)加入MgO的作用是调节溶液的pH,使Fe3+沉淀完全;滤渣的主要成分为BaSO4和Fe(OH)3
(5)向滤液中加入NaClO3饱和溶液后,发生反应的化学方程式为:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,再进一步制取Mg(ClO3)2•6H2O的实验步骤依次为①蒸发浓缩;②趁热过滤;③冷却结晶;④过滤、洗涤、干燥.
分析 卤块的成分有MgCl2•6H2O、MgSO4、FeCl2,加入双氧水之后,亚铁离子可以被氧化为三价铁离子,再向混合物中加入氯化钡溶液,可以将硫酸根离子转化为硫酸钡沉淀,加入氧化镁,调节pH=4,可以促进铁离子的水解,将铁离子转化为氢氧化铁而除去,过滤,得到的滤液是氯化镁,可以根据溶解度受温度的影响情况来获得要制取的物质,
(1)过滤实验用到的仪器:漏斗、玻璃棒、烧杯、滤纸、铁架台等;
(2)根据钡离子可以和硫酸根离子之间反应生成白色不溶于硝酸的白色沉淀来检验已沉淀完全;根据加氧化镁后溶液的pH为4,可以沉淀的离子来判断滤渣的主要成分;
(3)温度、固体颗粒大小、物质的浓度等会影响反应速率;
(4)金属氧化物MgO能与酸反应产生盐和水,所以加入MgO的作用是调节溶液的pH,使杂质Fe3+形成沉淀完全除去.根据示意图可知滤渣的主要成分为BaSO4和Fe(OH)3;
(5)利用NaCl、Mg(ClO3)2的溶解度与温度的关系,将溶液蒸发浓缩结晶、趁热过滤、冷却结晶,最后过滤、洗涤,得到Mg(ClO3)2•6H2O;
解答 解:卤块的成分有MgCl2•6H2O、MgSO4、FeCl2,加入双氧水之后,亚铁离子可以被氧化为三价铁离子,再向混合物中加入氯化钡溶液,可以将硫酸根离子转化为硫酸钡沉淀,加入氧化镁,调节pH=4,可以促进铁离子的水解,将铁离子转化为氢氧化铁而除去,过滤,得到的滤液是氯化镁,可以根据溶解度受温度的影响情况来获得要制取的物质,
(1)过滤实验用到的仪器:漏斗、玻璃棒、烧杯、滤纸、铁架台等,其中玻璃仪器有:漏斗、玻璃棒、烧杯,
故答案为:漏斗、玻璃棒、烧杯;
(2)检验硫酸根离子是否除净的方法:静置,取上层清液加入BaCl2,若无白色沉淀,则SO42-沉淀完全,加入氧化镁,调节溶液的pH为4,此时铁离子形成了沉淀氢氧化铁,钡离子已经和硫酸根离子只碱反应生成了硫酸钡沉淀,
故答案为:静置,取上层清液加入BaCl2,若无白色沉淀,则SO42-沉淀完全;
(3)影响化学反应速率的因素有:升高温度、将固体粉碎成细小的颗粒、增加物质的浓度等,因此加速卤块在KMnO4溶液中溶解的措施有:将卤块粉碎或加热等,
故答案为:将卤块粉碎或加热等;
(4)金属氧化物MgO能与酸反应产生盐和水.所以加入MgO的作用是调节溶液的pH,使杂质Fe3+形成沉淀完全除去.根据示意图可知滤渣的主要成分为BaSO4和Fe(OH)3,
故答案为:调节溶液的pH,使Fe3+沉淀完全;BaSO4和Fe(OH)3;
(5)利用NaCl、Mg(ClO3)2的溶解度与温度的关系将溶液蒸发浓缩、趁热过滤、冷却结晶,最后过滤、洗涤,就得到Mg(ClO3)2•6H2O,
故答案为:蒸发浓缩;冷却结晶.
点评 本题考查实验制备方案,涉及对操作的分析评价、物质的分离提纯、离子方程式书写、物质含量测定、氧化还原反应滴定等,是对学生综合能力的考查,难度中等.

| A. | H2CO3?2H++CO32- | B. | KHSO4?K++H++SO42- | ||
| C. | Ba(OH)2?Ba2++2OH- | D. | NaHCO3═Na++HCO3- |
| A. | HCl | B. | NaOH | C. | CuSO4 | D. | KNO3 |
| A. | 标准状况下2.24LO2 | B. | 含NA个氢原子的H2 | ||
| C. | 44gCO2 | D. | 含3.01×1023个分子的CH4 |
| A. | A、B中的氢的质量分数必相等 | |
| B. | A、B的实验式必相同 | |
| C. | A、B一定是同系物 | |
| D. | A、B可以是烃,也可以是烃的含氧衍生物 |
 已知A、B、C、D、E五种物质都含有相同的元素X,这五种物质间相互转化关系如下:
已知A、B、C、D、E五种物质都含有相同的元素X,这五种物质间相互转化关系如下: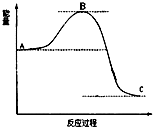 已知2SO2(g)十O2(g)$?_{催化剂}^{加热}$ 2SO3(g)反应过程的能量变化如图所示.请回答下列问题:
已知2SO2(g)十O2(g)$?_{催化剂}^{加热}$ 2SO3(g)反应过程的能量变化如图所示.请回答下列问题: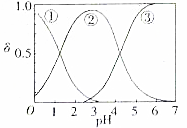 草酸、草酸盐在工业生产上用途非常广泛,H2C2O4水溶液中H2C2O4、HC2O4和C2O${\;}_{4}^{2-}$三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示.
草酸、草酸盐在工业生产上用途非常广泛,H2C2O4水溶液中H2C2O4、HC2O4和C2O${\;}_{4}^{2-}$三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示.