题目内容
11.某有机物的相对分子质量是94.5,取1.89g该有机物在氧气中充分燃烧,产生的气体依次通过浓硫酸和NaOH溶液,后者增重2.64g,用钠熔法测定含氯元素,经红外光谱分析有C-O、O-H等化学键,且存在手性碳原子,试写出该有机物的结构简式.分析 有机物的物质的量为$\frac{1.89g}{94.5g/mol}$=0.02mol,产生的气体依次通过浓硫酸和NaOH溶液,后者增重2.64g,为CO2的质量,且n(CO2)=$\frac{2.64}{44g/mol}$=0.06mol,则有机物含有3个C原子,用钠熔法测定含氯元素,经红外光谱分析有C-O、O-H等化学键,且存在手性碳原子,说明含有-OH,且含有Cl,分子式应为C3H7OCl,以此解答该题.
解答 解:有机物的物质的量为$\frac{1.89g}{94.5g/mol}$=0.02mol,产生的气体依次通过浓硫酸和NaOH溶液,后者增重2.64g,为CO2的质量,且n(CO2)=$\frac{2.64}{44g/mol}$=0.06mol,则有机物含有3个C原子,用钠熔法测定含氯元素,经红外光谱分析有C-O、O-H等化学键,且存在手性碳原子,说明含有-OH,且含有Cl,分子式应为C3H7OCl,则结构简式应为CH3CHClCH2OH,
答:该有机物的结构简式为CH3CHClCH2OH.
点评 本题考查有机物的推断,侧重考有机物分子式计算以及结构的判断,题目难度中等,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
1.某小组为研究电化学原理,设计如图装置,下列叙述不正确的是( )
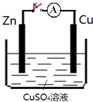

| A. | K打开,Zn片上会有金属铜析出 | |
| B. | 无论K是否闭合,锌片均会溶解,溶液均从蓝色逐渐变浅 | |
| C. | K闭合时,SO42-向铜电极移动 | |
| D. | K闭合时,电子从负极Zn流向正极 Cu,再从溶液中回到负极Zn |
2.下列叙述中能肯定说明金属A比金属B的活泼性强的是( )
| A. | A原子最外层电子数比B原子的最外层电子数少 | |
| B. | 由金属A和金属B构成的原电池,电子由A流向B | |
| C. | 1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 | |
| D. | 常温时,A能从酸中置换出氢,而B不能 |
19.下列化学用语或模型表示正确的是( )
| A. | H2O2分子结构式:H-O-O-H | B. | 氚原子符号:${\;}_{1}^{2}$H | ||
| C. | Mg2+结构示意图: | D. | CO2的电子式: |
6.下列叙述不正确的是( )
| A. | 在干旱地区植树造林时,可利用高吸水性树脂抗旱保水 | |
| B. | 硅酸钠的水溶液俗称水玻璃,是制备硅胶的原料 | |
| C. | SiO2的导电能力强,可用于制造太阳能电池板 | |
| D. | 服用阿司匹林若出现水杨酸反应,应立即停药并静脉滴注NaHCO3溶液. |
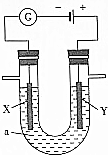 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: