题目内容
有一无色溶液,可能含有K+、Al3+、Mg2+、NH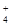 、Cl-
、SO
、Cl-
、SO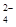 、HCO
、HCO 、Ba2+中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,只产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是(
)
、Ba2+中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,只产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是(
)
A.肯定没有NH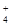 、HCO
、HCO 、Ba2+
、Ba2+
B.可能有K+、Cl- 、HCO
C.肯定有Al3+、Mg2+、SO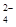 、NH
、NH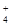
D.若另取部分原溶液,向其中加入足量AgNO3溶液有白色沉淀生成,证明原溶液中一定有Cl-
【答案】
A
【解析】溶液是无色的,则一定没有MnO4-;根据实验①可知,白色沉淀是氢氧化铝和氢氧化镁的混合物,因此一定含有A13+、Mg2+,所以没有HCO3-。气体无色无味肯定是氧气,没有NH4+;根据实验②可知,白色沉淀是硫酸钡,所以一定含有SO42-,不可能含有Ba2+;D选项鉴定氯离子应该用硝酸酸化的硝酸银溶液,排除。故答案为A

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目




 (1)在原溶液中一定不存在的离子有 ;
(1)在原溶液中一定不存在的离子有 ;
 等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。
等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。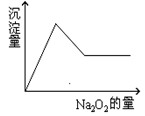

 (1)在原溶液中一定不存在的离子有
;
(1)在原溶液中一定不存在的离子有
;