题目内容
3.下列各组物质中,一定属于同系物的是( )| A. | 乙二醇 丙三醇 | B. | C6H5-OH C6H5CH2-OH | ||
| C. | C3H6 和C4H8 | D. | C2H6和C10H22 |
分析 结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;互为同系物的物质满足以下特点:结构相似、化学性质相似、分子式通式相同、分子式不同.
解答 解:A.乙二醇和丙三醇所含羟基个数不同,不属于同系物,故A错误;
B.C6H5-OH是酚类,C6H5-CH2OH是醇类,不是同一类物质,因此不属于同系物,故B错误;
C.C3H6 和C4H8可能为烯烃或环烷烃,因此不一定属于同系物,故C错误;
D.C2H6和C10H22满足CnH2n+2的通式属于烷烃,属于同系物,故D正确;
故选D.
点评 本题考查了同系物的概念与判断方法,难度不大,注意明确同系物的概念,明确同系物必须满足结构相似,有的物质之间满足相差一个或若干个CH2原子团,但结构不相似,就不属于同系物.

练习册系列答案
相关题目
11.除去下列物质中的少量杂质(括号内的物质为杂质),所选用的试剂或方法不正确的是( )
| A. | CO2(SO2):饱和NaHCO3溶液 | B. | NO(NO2):水 | ||
| C. | Cl2(HCl):NaOH溶液 | D. | Na2CO3固体(NaHCO3):加热 |
18.在不同温度下,水溶液中c (H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )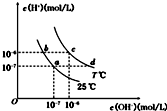

| A. | a点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42- | |
| B. | b点对应的溶液中大量存在:ClO-、Ba2+、OH-、I- | |
| C. | c点对应的溶液中大量存在:Na+、Ba2+、Cl- HCO3- | |
| D. | d点对应的溶液中大量存在:Na+、K+、SO32-、Cl- |
8.Se、Br两种元素的部分信息如图所示,下列说法正确的是( )
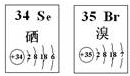

| A. | 原子半径:Br>Se>P | B. | 还原性:S 2 ->Se 2 ->Br - | ||
| C. | SeO 2既有氧化性又有还原性 | D. | 在Se2Br2分子中只含有极性键 |
13.下列电离方程式正确的是( )
| A. | NH3•H2O═NH4++OH- | B. | H2S?S2-+2H+ | ||
| C. | CaCO3?Ca2++CO32- | D. | CH3COONH4═CH3COO-+NH4+ |
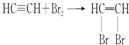
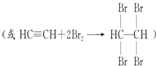 .
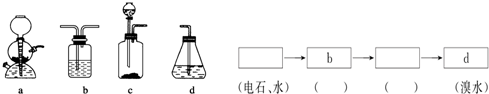
.
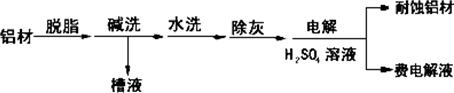
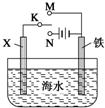 对金属制品进行抗腐蚀处理,可延长其使用寿命.
对金属制品进行抗腐蚀处理,可延长其使用寿命.