题目内容
为证明试管中盛有的少量溴乙烷中溴元素的存在,有下列实验操作步骤:①加入AgNO3溶液 ②加入 NaOH 醇溶液 ③加热 ④冷却 ⑤加稀硝酸至溶液呈酸性 ⑥加入 NaOH水溶液.
(1)选择最佳的操作顺序序号应该是
(2)写出有溴乙烷参加的化学反应的方程式: .
(1)选择最佳的操作顺序序号应该是
(2)写出有溴乙烷参加的化学反应的方程式:
考点:物质的检验和鉴别的实验方案设计
专题:物质检验鉴别题
分析:检验溴乙烷中溴元素,应在碱性条件下加热水解或碱性醇溶液条件下发生消去,最后加入硝酸酸化(因为阴离子在碱性条件下容易生成氢氧化银,迅速转变为氧化银沉淀,对后面的实验产生干扰,所以要先硝酸酸化,加入硝酸银,观察是否有黄色沉淀生成,以此来解答.
解答:
解:(1)证明溴乙烷中溴元素的存在,先加入⑥氢氧化钠溶液并③加热,发生水解反应生成NaBr,然后④冷却,再加入⑤稀硝酸至溶液呈酸性,最后加入①硝酸银溶液,生成淡黄色沉淀,则证明含溴元素,
即操作顺序为⑥③④⑤①,故答案为:⑥③④⑤①;
(2)溴乙烷参加的化学反应的方程式为CH3CH2Br+NaOH
CH3CH2OH+NaBr,故答案为:CH3CH2Br+NaOH
CH3CH2OH+NaBr.
即操作顺序为⑥③④⑤①,故答案为:⑥③④⑤①;
(2)溴乙烷参加的化学反应的方程式为CH3CH2Br+NaOH
| H2O |
| △ |
| H2O |
| △ |
点评:本题考查物质的鉴别和检验,为高频考点,把握卤代烃的性质及卤素离子的检验方法为解答的关键,侧重常见有机物性质的考查,注意水解液显碱性,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
天然水中含有细小悬浮颗粒或胶体颗粒,可用混凝剂进行净化处理,下述物质不属于天然水净化混凝剂的是( )
| A、硫酸铝 | B、硫酸亚铁 |
| C、硫酸镁 | D、聚合铝 |
在下列实验操作中错误的是( )
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计的水银球放置于蒸馏烧瓶的支管出口稍下处 |
| C、用容量瓶配制溶液时,加水超过了刻度线,没有采取补救措施,重新配制 |
| D、将5.85gNaCl溶于100mL水中,即配成1.0 mol/L NaCl溶液 |

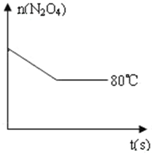 在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H>0,隔一段时间对该容器内的物质进行分析得到如下数据:
在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H>0,隔一段时间对该容器内的物质进行分析得到如下数据: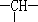 和一个-Cl,它可能的结构有
和一个-Cl,它可能的结构有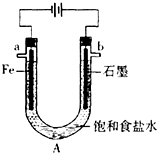 电解饱和食盐水装置的结构如图所示:
电解饱和食盐水装置的结构如图所示: