题目内容
3.下列物质的用途跟其化学性质相关的是( )| A. | 干冰用于人工降雨 | B. | 铁粉用于食品保存 | ||
| C. | 稀有气体用来制作电光源 | D. | 铜用作电线 |
分析 物质的物理性质是不需要通过化学变化表现出来的性质,比如硬度、密度、溶解度、熔沸点等,物质的化学性质是通过化学反应表现出来的性质,比如氧化性、可燃性、稳定性等,据此解答即可.
解答 解:A.干冰用于人工降雨,利用的是干冰升华吸热的性质,不是化学性质,故A错误;
B.铁粉用于食品保存,利用的是铁粉与氧气和水反应的性质,属于化学性质,故B正确;
C.稀有气体用来制作电光源,该性质不是通过化学反应表现出来的,故C错误;
D.铜用作电线,利用的是金属导电的性质,不是化学性质,故D错误,
故选B.
点评 本题主要考查的是物理性质与化学性质的区别以及常见物质的用途,难度不大,掌握基础是关键.

练习册系列答案
相关题目
13.研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果.下列表达不正确的是( )
| A. | CO2通入澄清的石灰水中反应的产物 $\frac{n(C{O}_{2})}{n[Ca(OH)_{2}]}$ $\frac{n(C{O}_{2})}{n[Ca(OH)_{2}]}$ | |
| B. | Fe在Cl2中的燃烧产物: $\frac{n(C{l}_{2})}{n(Fe)}$ $\frac{n(C{l}_{2})}{n(Fe)}$ | |
| C. | AlCl3溶液中滴加NaOH后铝的存在形式: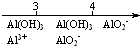 $\frac{n(NaOH)}{n(AlC{l}_{3})}$ $\frac{n(NaOH)}{n(AlC{l}_{3})}$ | |
| D. | 氨水与SO2反应后溶液中的铵盐: $\frac{n(N{H}_{3}{H}_{2}O)}{n(S{O}_{2})}$11 $\frac{n(N{H}_{3}{H}_{2}O)}{n(S{O}_{2})}$11 |
11.足量MnO2与VmL 10mol/L的盐酸共热制氯气,在标准状况下制2.24LCl2则V的取值为( )
| A. | V>40 | B. | 20<V<40 | C. | V=40 | D. | V=20 |
18.在一密闭容器中进行反应 X2(g)+3Y2(g)?2Z2(g),若 X2、Y2、Z2的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,当反应达到平衡后,各物质的浓度有可能是( )
| A. | c(X2)=0.2 mol/L | B. | c(Y2)=0.1 mol/L | C. | c(Z2)=0.4 mol/L | D. | c(Y2)=0.6 mol/L |
8.下列各组物质中,分类完全正确的一组是( )
| A酸 | B碱 | C盐 | D氧化物 |
| H2SO4 | Ba(OH)2 | H2S | H2O2 |
| NaHCO3 | Cu2(OH)2CO3 | KCl | CO |
| HNO3 | NaOH | CaCO3 | CuO |
| HCl | Na2CO3 | CuSO4 | MnO2 |
| A. | A | B. | B | C. | C | D. | D |
15.下列关于反应热和焓变的说法正确的是( )
| A. | 反应热就是反应中放出的热量 | |
| B. | 当反应放热时△H>0,反应吸热时△H<0 | |
| C. | 一个化学反应中,当反应物的总能量大于生成物的总能量时,反应放热,△H为“-” | |
| D. | 一个化学反应中,生成物总键能大于反应物的总键能时,反应吸热,△H为“+” |
12.下列化学用语正确的是( )
| A. | 甲醛的结构式:HCHO | B. | 丙烷分子的比例模型: | ||
| C. | 四氯化碳分子的电子式: | D. | 2-乙基-1,3-丁二烯分子的键线式: |
13.下列说法中正确的是( )
| A. | 元素周期表的七个周期永远不会改变 | |
| B. | 元素周期表有九个横行,分为七个周期 | |
| C. | 元素周期表有十八个纵行,分为十六个族 | |
| D. | 元素周期表有十八个纵行,分为十八个族 |