题目内容
某无色溶液中可能含有离子:Na+、Ag+、Fe3+、Ba2+、Al3+、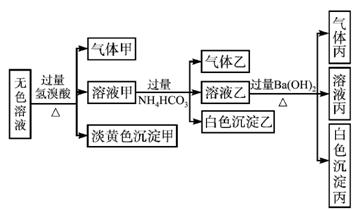
图1-1-6
(1)沉淀甲为________(填化学式),生成沉淀甲的离子方程式:________________。
(2)沉淀乙为________ (填化学式),由溶液甲生成沉淀乙的离子方程式:________________。
(3)沉淀丙可能是________ (填化学式)。
(4)气体甲的成分有哪几种可能,答:①________,②________,③________ (有多少种就填多少种,可以填不满)。
(5)综合上述信息可以确定肯定存在的离子有________________________________。
解析:由溶液是无色的,排除了Fe3+,能和氢溴酸反应生成气体和淡黄色沉淀,可知一定有![]() 、S2-,排除Ag+、Ba2+、Al3+。淡黄色沉淀应是单质硫。溶液中加入过量的氢溴酸后呈现酸性,再加入过量的碳酸氢铵,由产生的现象可知白色沉淀乙应是氢氧化铝,气体乙可能是二氧化碳,溶液乙一定含有
、S2-,排除Ag+、Ba2+、Al3+。淡黄色沉淀应是单质硫。溶液中加入过量的氢溴酸后呈现酸性,再加入过量的碳酸氢铵,由产生的现象可知白色沉淀乙应是氢氧化铝,气体乙可能是二氧化碳,溶液乙一定含有![]() 、
、![]() 、Br-,然后加入过量的氢氧化钡产生的白色沉淀可能是碳酸钡,也可能是硫酸钡。气体丙应是氨气。
、Br-,然后加入过量的氢氧化钡产生的白色沉淀可能是碳酸钡,也可能是硫酸钡。气体丙应是氨气。
答案:(1)S 2S2-+![]() +6H+====3S↓+3H2O
+6H+====3S↓+3H2O
(2)Al(OH)3 Al3++3![]() ====Al(OH)3?↓+3CO2↑
====Al(OH)3?↓+3CO2↑
(3)BaCO3或BaSO4和BaCO3
(4)①H2S ②SO2 (5)S2-、![]() 、
、![]() 、Na+
、Na+

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
(2011?河西区一模)某无色溶液中可能含有 ①Na+、②Ba2+、③Cl-、④Br-、⑤SO42-、⑥SO32-离子中的若干种,依顺序进行下列实验,且每步所加试剂均过量,观察到的现象如下:
|
某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液呈无色,则下列关于溶液组成的判断正确的是( )
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32-④可能含有I-.
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32-④可能含有I-.
| A、①③ | B、①②③ | C、③④ | D、②③④ |
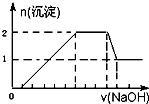 某无色溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列说法一定正确的是( )
某无色溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列说法一定正确的是( )| A、一定存在H+、Mg2+、Al3+、NH4+,一定不存在Na+、SO42-、Fe3+ | B、一定存在H+、Al3+、NH4+、SO42-,可能存在Na+、Mg2+ | C、溶液中c(H+):c(Al3+):c(Mg2+)为1:1:1 | D、溶液中c(H+):c(SO42-)为2:9 |