题目内容
15.看反应物或产物的配比是否正确.如稀H2SO4和Ba(OH)2溶液反应不能写成H++OH-+SO42-+Ba2+═BaSO4↓+H2O,应写成Ba2++2H++20H-+SO42-=BaSO4↓+2H2O.分析 硫酸与氢氧化钡反应生成硫酸钡和水,反应的实质为,钡离子与氢氧根离子与氢离子,成水,钡离子与硫酸根离子生成硫酸钡沉淀,离子方程式不能写成H++OH-+SO42-+Ba2+═BaSO4↓+H2 0,因为1个钡离子对应2个氢氧根离子,离子个数配比不符合物质结构,据此解答.
解答 解:硫酸与氢氧化钡反应生成硫酸钡和水,反应的实质为,钡离子与氢氧根离子与氢离子,成水,钡离子与硫酸根离子生成硫酸钡沉淀,离子方程式不能写成H++OH-+SO42-+Ba2+═BaSO4↓+H2 0,因为1个钡离子对应2个氢氧根离子,离子个数配比不符合物质结构,正确的离子方程式应为:Ba2++2H++20H-+SO42-=BaSO4↓+2H2O,
故答案为:Ba2++2H++20H-+SO42-=BaSO4↓+2H2O.
点评 本题考查了离子方程式书写,明确反应实质及离子方程式书写方法是解题关键,注意书写离子方程式时,离子个数配比应符合物质结构,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.某工业废水仅含下表中的某些离子,且各种离子的物质的量浓度相等,均为0.1mol/L(此数值忽略水的电离及离子的水解).
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取该无色溶液5mL,滴加一滴氨水有沉淀生成,且离子种类增加.
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰.
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.下列推断不正确的是( )
| 阳离子 | K+ Ag+ Mg2+ Cu2+ Al3+ NH4+ |
| 阴离子 | Cl- CO32- NO3- SO42- I- |
Ⅰ.取该无色溶液5mL,滴加一滴氨水有沉淀生成,且离子种类增加.
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰.
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.下列推断不正确的是( )
| A. | 由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、NH4+、Cu2+ | |
| B. | Ⅲ中加入盐酸生成无色气体的离子方程式是6I-+2NO3-+8H+═3I2+2NO↑+4H2O | |
| C. | 原溶液一定只含有的离子I-、NO3-、SO42-、Mg2+、Al3+ | |
| D. | 另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体质量为0.4g |
3.下列物质所属的类别正确的是( )
| A. | 纯碱--盐 | B. | 干冰--混合物 | ||
| C. | 澄清石灰水--纯净物 | D. | 洁净的空气--纯净物 |
11.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是Ar(填元素符号)
(2)②③⑦三种元素的原子半径从大到小的顺序为Cl>N>O(填元素符号)
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式HClO4,碱性最强的化合物的名称氢氧化钾.
(4)元素⑤的氧化物与元素④的最高价氧化物对应水化物反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O.
(5)元素⑥和⑦形成的气态氢化物较稳定是HCl(填化学式),用方程式来说明元素⑦的非金属性比⑥的非金属强的事实Cl2+H2S=S↓+2HCl(一个或两个方程式均可)
(6)表示①与③形成的化合物的电子式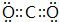 ,写出它的一种用途做灭火剂等.
,写出它的一种用途做灭火剂等.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | Ⅵ | VⅡA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)②③⑦三种元素的原子半径从大到小的顺序为Cl>N>O(填元素符号)
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式HClO4,碱性最强的化合物的名称氢氧化钾.
(4)元素⑤的氧化物与元素④的最高价氧化物对应水化物反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O.
(5)元素⑥和⑦形成的气态氢化物较稳定是HCl(填化学式),用方程式来说明元素⑦的非金属性比⑥的非金属强的事实Cl2+H2S=S↓+2HCl(一个或两个方程式均可)
(6)表示①与③形成的化合物的电子式
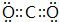 ,写出它的一种用途做灭火剂等.
,写出它的一种用途做灭火剂等.
13.室温下由水电离出的H+的浓度是1×10-12mol/L,则该溶液( )
| A. | 一定是酸性溶液 | B. | 一定是碱性溶液 | ||
| C. | 可能是中性溶液 | D. | 可能是酸性溶液也可能是碱性溶液 |