题目内容
在11P4+60CuSO4+96H2O=24H3PO4+20Cu3P+60H2SO4反应中,若有11molP4参加反应,则被CuSO4氧化的P4的物质的量为( )
| A、11mol | B、44mol | C、3mol | D、6mol |
分析:氧化还原反应中:失电子化合价升高的元素所在的反应物是还原剂,还原剂发生氧化反应.,化合价降低的物质作氧化剂发生还原反应;
该氧化还原反应中Cu元素的化合价由+2价降低到+1价,硫酸铜是氧化剂,P4部分磷元素由0价降低到-3价,部分磷元素由0价升高到+5价,磷元素的化合价既升高又降低,所以P4既是氧化剂又是还原剂,若有11molP4参加反应,其中5mol的P4做氧化剂,60mol硫酸铜做氧化剂,只有6mol的P4做还原剂,60mol的CuSO4可氧化5mol的P4,则11molP4参加反应,被CuSO4氧化的P4的物质的量为3mol.
该氧化还原反应中Cu元素的化合价由+2价降低到+1价,硫酸铜是氧化剂,P4部分磷元素由0价降低到-3价,部分磷元素由0价升高到+5价,磷元素的化合价既升高又降低,所以P4既是氧化剂又是还原剂,若有11molP4参加反应,其中5mol的P4做氧化剂,60mol硫酸铜做氧化剂,只有6mol的P4做还原剂,60mol的CuSO4可氧化5mol的P4,则11molP4参加反应,被CuSO4氧化的P4的物质的量为3mol.
解答:解:反应11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4中,Cu元素的化合价由+2价降低到+1价,硫酸铜是氧化剂,P4部分磷元素由0价降低到-3价,部分磷元素由0价升高到+5价,磷元素的化合价既升高又降低,所以P4既是氧化剂又是还原剂,若有11molP4参加反应,其中磷元素由0价降低到-3价做氧化剂,5mol的P4做氧化剂,电子的物质的量=20×3mol=60mol,磷元素由0价升高到+5价做还原剂,6mol的P4做还原剂,失去电子的物质的量=24×(5-0)mol=120mol,Cu元素的化合价由+2价降低到+1价,60mol硫酸铜做氧化剂,1mol的P4做还原剂失去电子的物质的量为20mol,所以被硫酸铜氧化的P4的物质的量为
=3mol,
故选C.
| 60mol |
| 20 |
故选C.
点评:本题考查氧化还原反应,根据氧化还原反应中磷元素化合价的变化和硫酸铜中铜元素的化合价变化情况来找出硫酸铜和P4的关系是解答本题的关键,题目难度中等.

练习册系列答案
相关题目

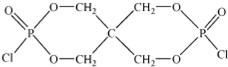
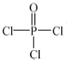 )与季戊四醇(
)与季戊四醇(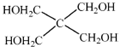 )以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体.季戊四醇与X 的核磁共振氢谱如图所示.
)以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体.季戊四醇与X 的核磁共振氢谱如图所示.