题目内容
4.利用海水提取溴和镁的过程如下,下列说法不正确的是 ( )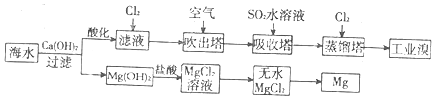
| A. | 若提取1 mol Br2,至少需要标准状况下44.8 L的Cl2 | |
| B. | 工业上常利用电解熔融MgCl2冶炼金属镁 | |
| C. | 富集溴元素过程中,空气吹出法利用了溴易挥发的性质 | |
| D. | 工业溴中含少量Cl2,可用氢氧化钠溶液除去 |
分析 海水中加入氢氧化钙沉淀镁离子生成氢氧化镁沉淀,过滤后在沉淀中加入盐酸溶解,得到氯化镁溶液,通过浓缩蒸发,冷却结晶得到氯化镁晶体,在氯化氢气流中加热失水得到无水氯化镁,电解熔融氯化镁得到金属镁;海水浓缩晒盐得到卤水中通入氧化剂氯气氧化溴离子得到溴单质,2Br-+C12=Br2+2Cl-,吹入热的空气用二氧化硫吸收富集溴SO2+Br2+2H2O=4H++2Br-+SO42-,通入氯气发生氧化还原反应生成单质溴.以此解答该题.
解答 解:A.若提取1 mol Br2,依据2Br-+Cl2=Br2+2Cl-,提取粗溴消耗氯气物质的量为1mol,得到纯溴需氯气物质的量为1mol,所以在标准状况下体积为V=nVm=2mol×224.4L/mol=44.8 L,故A正确;
B.从MgCl2溶液中得到MgCl2固体,电解熔融氯化镁得到金属镁和氯气,反应的化学方程式为:MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑,故B正确;
C.海水提取溴一般用氯气置换溴离子转化为溴单质,用空气和水蒸气吹出单质溴,再用SO2将其还原吸收转化为HBr,达到富集的目的,故C正确;
D.工业溴中含少量Cl2,用NaOH溶液除去,溴和氢氧化钠反应生成溴化钠、次溴酸钠和水,反应的化学方程式为Br2+2NaOH═NaBr+NaBrO+H2O,溴被除去,故D错误.
故选D.
点评 本题考查了海水资源的综合应用,为高频考点,涉及物质的分离提纯等知识,侧重于化学与生活的综合运用,培养了学生运用知识分析问题的能力,题目难度中等.

练习册系列答案
相关题目
15.铁、铜单质及其化合物应用范围很广.现有含氯化亚铁杂质的氯化铜晶体(CuCl2•2H2O),为制取纯净的 CuCl2•2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
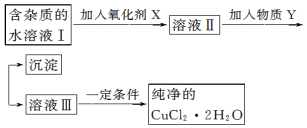
已知Cu2+、Fe3+和 Fe2+的氢氧化物开始沉淀和沉淀完全时的 pH,见表:
请回答下列问题:
(1)常温下,计算 Fe(OH)3的溶度积Ksp=10-38(mol•L-1)4(通常认为残留在溶液中的离子浓度小于1×10-5mol/L 时则沉淀完全.)
(2)加入氧化剂的目的将Fe2+氧化成Fe3+,便于生成沉淀与Cu2+分离.
(3)最适合作氧化剂X的是C.
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(4)加入的物质 Y 是CuO(或Cu(OH)2、CuCO3、Cu2(OH)2CO3).
(5)若向溶液Ⅱ中加入碳酸钙,产生的现象是碳酸钙溶解,产生气泡和红褐色沉淀.

已知Cu2+、Fe3+和 Fe2+的氢氧化物开始沉淀和沉淀完全时的 pH,见表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的 pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的 pH | 3.0 | 9.0 | 6.7 |
(1)常温下,计算 Fe(OH)3的溶度积Ksp=10-38(mol•L-1)4(通常认为残留在溶液中的离子浓度小于1×10-5mol/L 时则沉淀完全.)
(2)加入氧化剂的目的将Fe2+氧化成Fe3+,便于生成沉淀与Cu2+分离.
(3)最适合作氧化剂X的是C.
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(4)加入的物质 Y 是CuO(或Cu(OH)2、CuCO3、Cu2(OH)2CO3).
(5)若向溶液Ⅱ中加入碳酸钙,产生的现象是碳酸钙溶解,产生气泡和红褐色沉淀.
12.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 18 g H2O含有的氢原子数目为NA | |
| B. | 标准状况下,22.4LCO2含有的分子数目为NA | |
| C. | 1mol•L-1K2SO4溶液中含有的钾离子数目为2NA | |
| D. | 1mol H2在O2中完全燃烧转移的电子数目为NA |
19.下列物成中,不属于电解质的是( )
| A. | 蔗糖 | B. | NaCl | C. | NaOH | D. | H2SO4 |
9.下列有关物质检验的操作、现象及结论均正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水中,变石灰水浑浊 | 该溶液中一定含有CO32- |
| C | 向无色溶液中滴加氯水,再加CCl4振荡、静置、溶液分层,下层呈紫红色 | 该溶液中一定含有I- |
| D | 取洁净的铂丝在酒精灯火焰上灼烧至无色,再蘸取少量溶液置于火焰上灼烧,火焰呈黄色,通过蓝色钴玻璃观察,火焰呈紫色 | 该溶液一定含有Na+、K+ |
| A. | A | B. | B | C. | C | D. | D |
16.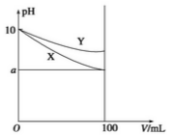 常温下,pH=10 的X、Y 两种碱溶液各1mL,分别稀释到100mL,其pH 与溶液体积(V)的关系如图所示,下列说法正确的是( )
常温下,pH=10 的X、Y 两种碱溶液各1mL,分别稀释到100mL,其pH 与溶液体积(V)的关系如图所示,下列说法正确的是( )
 常温下,pH=10 的X、Y 两种碱溶液各1mL,分别稀释到100mL,其pH 与溶液体积(V)的关系如图所示,下列说法正确的是( )
常温下,pH=10 的X、Y 两种碱溶液各1mL,分别稀释到100mL,其pH 与溶液体积(V)的关系如图所示,下列说法正确的是( )| A. | 若8<a<10,则X、Y 都是弱碱 | |
| B. | 稀释后,X 溶液的碱性比Y 溶液的碱性强 | |
| C. | X、Y 两种碱溶液中溶质的物质的量浓度一定相等 | |
| D. | 分别完全中和X、Y 这两种碱溶液时,消耗同浓度盐酸的体积VX>VY |
13.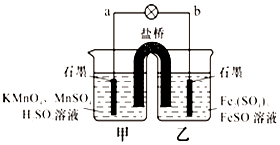 某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( )
某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( )
 某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( )
某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( )| A. | 外电路的电流方向是从a到b | |
| B. | 甲烧杯中溶液的pH逐渐减小 | |
| C. | 电池工作时,盐桥中的SO42-移向甲烧杯 | |
| D. | 乙烧杯中发生还原反应 |
 某化学兴趣小组用FeCl2(用铁粉与盐酸反应制得)和NH4HCO3制备FeCO3的装置示意图如图所示.回答下列问题:
某化学兴趣小组用FeCl2(用铁粉与盐酸反应制得)和NH4HCO3制备FeCO3的装置示意图如图所示.回答下列问题: