题目内容
下将稀NaOH溶液和稀CH3COOH混合,不可能出现的结果是( )
| A、pH>7,且c (OH-)>c (Na+)>c (H+)>c (CH3COO-) |
| B、pH>7,且c (Na+)+c (H+)=c (CH3COO-)+c (OH-) |
| C、PH<7,且c (CH3COO-)>c (H+)>c (Na+)>c (OH-) |
| D、pH=7,且c (CH3COO-)>c (Na+)>c (H+)=c (OH-) |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A.氢离子和氢氧根离子反应生成水,钠离子不参加反应,则c(OH-)<c (Na+);
B.任何电解质溶液都存在电荷守恒,根据电荷守恒判断;
C.常温下,pH<7,说明溶液呈酸性,当醋酸的物质的量远远大于氢氧化钠时,则c(CH3COO-)>c(H+)>c(Na+);
D.常温下,pH=7,溶液为中性,则c (H+)=c(OH-),根据电荷守恒可得:c(CH3COO-)=c(Na+).
B.任何电解质溶液都存在电荷守恒,根据电荷守恒判断;
C.常温下,pH<7,说明溶液呈酸性,当醋酸的物质的量远远大于氢氧化钠时,则c(CH3COO-)>c(H+)>c(Na+);
D.常温下,pH=7,溶液为中性,则c (H+)=c(OH-),根据电荷守恒可得:c(CH3COO-)=c(Na+).
解答:
解:A.氢离子和氢氧根离子反应生成水,钠离子不反应,所以c(Na+)>c(OH-),不能出现c(OH-)>c(Na+),故A错误;
B.任何电解质溶液都存在电荷守恒,根据电荷守恒得:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),故B正确;
C.常温下,pH<7,说明溶液呈酸性,当醋酸的物质的量远远大于氢氧化钠时,溶液显示酸性,且满足:c(CH3COO-)>c(H+)>c(Na+),故C正确;
D.常温下,混合液的pH=7,说明溶液呈中性,则c(OH-)=c(H+),根据电荷守恒c(Na+)+c(H+)=c(OH-)+c(CH3COO-)可得:c(CH3COO-)=c (Na+),溶液中离子浓度关系为:c(CH3COO-)=c(Na+)>c(H+)=c(OH-),故D错误;
故选AD.
B.任何电解质溶液都存在电荷守恒,根据电荷守恒得:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),故B正确;
C.常温下,pH<7,说明溶液呈酸性,当醋酸的物质的量远远大于氢氧化钠时,溶液显示酸性,且满足:c(CH3COO-)>c(H+)>c(Na+),故C正确;
D.常温下,混合液的pH=7,说明溶液呈中性,则c(OH-)=c(H+),根据电荷守恒c(Na+)+c(H+)=c(OH-)+c(CH3COO-)可得:c(CH3COO-)=c (Na+),溶液中离子浓度关系为:c(CH3COO-)=c(Na+)>c(H+)=c(OH-),故D错误;
故选AD.
点评:本题考查了酸碱混合的定性判断、离子浓度大小的比较,题目难度中等,明确溶液中存在的溶质及其性质是解本题关键,并结合溶液的酸碱性、电荷守恒来分析解答,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的密闭容器中,发生反应:2SO2+O2?2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是( )
| A、2 mol SO2+1 mol O2 |
| B、4 mol SO2+1 mol O2 |
| C、2 mol SO2+1 mol O2+2 SO3 |
| D、3 mol SO2+1 mol O2+1 SO3 |
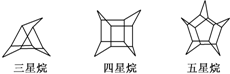 化学家们合成了如图所示的一系列的星烷.下列说法正确的是( )
化学家们合成了如图所示的一系列的星烷.下列说法正确的是( )| A、它们的一氯代物均只有三种 |
| B、它们之间互为同系物 |
| C、三星烷与乙苯互为同分异构体 |
| D、六星烷的化学式为C18H24 |
分子式为CNH2NO2的羧酸和某醇酯化生成分子式为CN+2H2N+4O2的酯,反应所需羧酸和醇的质量比为1:1,则该羧酸是( )
| A、乙酸 | B、丙酸 | C、甲酸 | D、乙二酸 |
下列各组离子一定能大量共存的是( )
| A、在含有大量[Al(OH)4]-溶液中NH4+、Na+、Cl-、H+ |
| B、在强碱溶液中 Na+、K+、CO32-、NO3- |
| C、在pH=12的溶液中 NH4+、Na+、SO42-、Cl- |
| D、在c(H+)=0.1 mol?L-1的溶液中K+、I-、Cl-、NO3- |
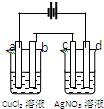 如图,以惰性电极材料为电极进行电解,在a、b、c、d各电极上析出生成物的物质的量比例关系正确的是( )
如图,以惰性电极材料为电极进行电解,在a、b、c、d各电极上析出生成物的物质的量比例关系正确的是( )| A、1:1:1:1 |
| B、2:2:1:1 |
| C、2:2:4:1 |
| D、1:2:2:4 |
下列关于实验操作的说法正确的是( )
| A、学生甲认为苯酚不慎沾在皮肤上时,根据苯酚能够与65℃以上的水任意比混溶,所以最好马上用65℃以上的水进行洗涤 |
| B、学生乙在做酸碱中和滴定实验时,将标准液盐酸溶液通过移液管移入锥形瓶,并滴加1-2滴酚酞作为指示剂,而待测液氢氧化钠溶液装入碱式滴定管进行滴定 |
| C、学生丙在称量某固体样品的质量时,托盘一端放入5克砝码,并将游码用镊子沿着刻度尺向盛样品的一端移动后,停在1.2克和1.3克偏右的某一处时,天平平衡,该生马上得到该样品的质量为6.3克 |
| D、学生丁在做中和热测定时,认为应用稀的含等物质的量的H+和OH-的溶液反应来进行测定 |