题目内容
下列与阿伏加德罗常数的值(NA)有关的说法正确的是( )
| A、NA个Fe(OH)3胶体粒子的质量为107g |
| B、3mol NF3与水完全反应生成HNO3和NO,转移电子数2NA |
| C、标准状况下,2.24L Cl2溶于水中达到饱和,可得到HClO分子的数目是0.1NA |
| D、常温常压下,1.7g H2O2中含有的电子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氢氧化铁胶粒为氢氧化铁的聚集体,无法计算氢氧化铁胶粒的质量;
B.根据电子守恒,3mol NF3与水完全反应生成1molHNO3和2molNO,转移了2mol电子;
C.氯气与水的反应中,只有少量的氯气与水反应生成氯化氢和次氯酸;
D.双氧水中含有18个电子,1.7g双氧水的物质的量为0.05mol,含有0.9mol电子.
B.根据电子守恒,3mol NF3与水完全反应生成1molHNO3和2molNO,转移了2mol电子;
C.氯气与水的反应中,只有少量的氯气与水反应生成氯化氢和次氯酸;
D.双氧水中含有18个电子,1.7g双氧水的物质的量为0.05mol,含有0.9mol电子.
解答:
解:A.氢氧化铁胶粒为氢氧化铁的聚集体,无法计算NA个Fe(OH)3胶体粒子的质量,故A错误;
B.由电子守恒可知:3mol NF3与水完全反应生成1molHNO3和2molNO,转移了2mol电子,转移电子数2NA,故B正确;
C.标准状况下,2.24L Cl2的物质的量为0.1mol,0.1mol氯气溶于水,只有少量的氯气与水反应生成次氯酸和氯化氢,所以生成的次氯酸小于0.1mol,HClO分子的数目小于0.1NA,故C错误;
D.1.7g双氧水的物质的量为0.05mol,0.05mol双氧水中含有0.9mol电子,含有的电子数为0.9NA,故D错误;
故选B.
B.由电子守恒可知:3mol NF3与水完全反应生成1molHNO3和2molNO,转移了2mol电子,转移电子数2NA,故B正确;
C.标准状况下,2.24L Cl2的物质的量为0.1mol,0.1mol氯气溶于水,只有少量的氯气与水反应生成次氯酸和氯化氢,所以生成的次氯酸小于0.1mol,HClO分子的数目小于0.1NA,故C错误;
D.1.7g双氧水的物质的量为0.05mol,0.05mol双氧水中含有0.9mol电子,含有的电子数为0.9NA,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确氢氧化铁胶粒为氢氧化铁的聚集体,要求学生掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项C为易错点,注意次氯酸与水的反应中,只有少量的氯气与水反应生成氯化氢和次氯酸.

练习册系列答案
相关题目
已知101kPa下,1mol石墨转化为金刚石要吸收热量1.895kJ.据此推理所得到的下列结论中,正确的是( )
| A、金刚石比石墨稳定 |
| B、石墨转化为金刚石是物理变化 |
| C、石墨的能量比金刚石的能量高 |
| D、由石墨制备金刚石一定是吸热反应 |
为“绿色奥运”某同学提出了下列环保建议,其中你认为可以采纳的是( )
①用气态燃料代替液态和固态燃料作为发动机动力来源;②开发生产无汞电池;③提倡使用一次性塑料餐具和塑料袋,以防传染疾病;④分类回收垃圾;⑤开发无磷洗涤剂;⑥提倡使用手帕,减少餐巾纸的使用.
①用气态燃料代替液态和固态燃料作为发动机动力来源;②开发生产无汞电池;③提倡使用一次性塑料餐具和塑料袋,以防传染疾病;④分类回收垃圾;⑤开发无磷洗涤剂;⑥提倡使用手帕,减少餐巾纸的使用.
| A、①③③④ | B、②③④⑤ |
| C、①②④⑤⑥ | D、全部 |
现有Na2CO3、H2SO4、Ba(OH)2三种物质的量浓度与体积都相等的溶液,若以不同顺序将它们中的两种混合起来,出现沉淀后过滤,再将滤液与第三种溶液混合起来,最终所得的溶液( )
| A、一定呈酸性 |
| B、可能呈碱性 |
| C、可能呈中性 |
| D、一定呈中性 |
下面是生产生活中的常见有机物的分子式、结构(简)式或名称:下列有关说法正确的是( )
① ②
② ③
③ ④
④ ⑤CH3CH2OH ⑥C6H12O6 ⑦CH3COOH ⑧硬脂酸甘油酯 ⑨蛋白质 ⑩聚乙烯.
⑤CH3CH2OH ⑥C6H12O6 ⑦CH3COOH ⑧硬脂酸甘油酯 ⑨蛋白质 ⑩聚乙烯.
①
 ②
② ③
③ ④
④ ⑤CH3CH2OH ⑥C6H12O6 ⑦CH3COOH ⑧硬脂酸甘油酯 ⑨蛋白质 ⑩聚乙烯.
⑤CH3CH2OH ⑥C6H12O6 ⑦CH3COOH ⑧硬脂酸甘油酯 ⑨蛋白质 ⑩聚乙烯.| A、能与溴的四氯化碳溶液发生加成反应并使之褪色的一定有①②④⑩ |
| B、投入钠一定能产生H2的是⑤⑦⑧⑨ |
| C、含碳量最高、有毒、常温下为液体且点燃时有浓的黑烟的是① |
| D、属于高分子材料的是⑧⑨⑩ |
下列关于甲烷性质的叙述,不正确的是( )
| A、甲烷在空气中燃烧生成水和二氧化碳 |
| B、甲烷是无色、有臭味的气体 |
| C、甲烷是一种简单的有机物 |
| D、甲烷极难溶于水 |
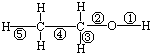 乙醇分子中不同的化学键如图.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )
乙醇分子中不同的化学键如图.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )| A、与金属钠反应时,键①断裂 |
| B、在Ag催化下与O2反应时,键①、③断裂 |
| C、与CuO反应时,键①断裂 |
| D、与浓硫酸共热至140℃时,键①或键②断裂;共热至170℃时,键②、⑤断裂 |
常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A、在碱性溶液中:K+、Cl-、Na+、CO32- | ||||
B、在
| ||||
| C、澄清透明溶液中:Cu2+、Fe3+、I-、SO42- | ||||
D、与铝粉反应放出氢气的无色溶液中:K+、N
|
下列说法正确的是( )
| A、海水中含量最高的元素是氯 |
| B、海水中含量最高的物质是氯化钠 |
| C、加碘食盐溶液遇淀粉溶液显蓝色 |
| D、加碘食盐中的碘是含碘元素的化合物 |