题目内容
一定温度下,将1mol X和1mol Y气体充入2L恒容密闭容器,发生反应X(g)+Y(g)?mZ(g)+Q(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体Z的浓度随时间变化如图所示.下列说法正确的是( )

| A.反应方程式中的m=1 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是移去少量物质Q |
| D.t1~t3间该反应的平衡常数均为4 |

A、由图可知,t2时刻Z的浓度增大,但平衡不移动,故改变的条件应是增大压强,反应前后气体的化学计量数之和相等,故m=1+1=2,故A错误;
B、催化剂不能影响物质的浓度,由图可知,t2时刻Z的浓度增大,但平衡不移动,故改变的条件应是增大压强,故B错误;
C、Q是固体,改变Q的用量,不影响平衡移动,t3时刻改变的条件,瞬间Z的浓度不变,平衡向正反应移动,可能是增大反应物的浓度或升高温度,故C错误;
D、t1~t3间温度相同,由图可知t1时刻平衡时,c(Z)=0.5mol/L,则:
X(g)+Y(g)?2Z(g)+Q(s),
开始(mol/L):0.5 0.5 0
变化(mol/L):0.25 0.25 0.5
平衡(mol/L):0.25 0.25 0.5
故平衡常数为
=4,故D正确;
故选D.
B、催化剂不能影响物质的浓度,由图可知,t2时刻Z的浓度增大,但平衡不移动,故改变的条件应是增大压强,故B错误;
C、Q是固体,改变Q的用量,不影响平衡移动,t3时刻改变的条件,瞬间Z的浓度不变,平衡向正反应移动,可能是增大反应物的浓度或升高温度,故C错误;
D、t1~t3间温度相同,由图可知t1时刻平衡时,c(Z)=0.5mol/L,则:
X(g)+Y(g)?2Z(g)+Q(s),
开始(mol/L):0.5 0.5 0
变化(mol/L):0.25 0.25 0.5
平衡(mol/L):0.25 0.25 0.5
故平衡常数为
| 0.5×0.5 |
| 0.25×0.25 |
故选D.

练习册系列答案
相关题目
 (2012?通州区一模)一定温度下,将1mol X和1mol Y气体充入2L恒容密闭容器,发生反应X(g)+Y(g)?mZ(g)+Q(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体Z的浓度随时间变化如图所示.下列说法正确的是( )
(2012?通州区一模)一定温度下,将1mol X和1mol Y气体充入2L恒容密闭容器,发生反应X(g)+Y(g)?mZ(g)+Q(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体Z的浓度随时间变化如图所示.下列说法正确的是( )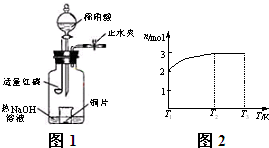 X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成.X有5个原子核.通常状况下,W为无色液体.已知:X+Y
X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成.X有5个原子核.通常状况下,W为无色液体.已知:X+Y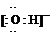
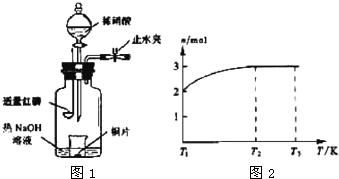 (2008?北京)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核.通常状况下,W为无色液体.
(2008?北京)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核.通常状况下,W为无色液体.