题目内容
X、Y、Z、W均为短周期元素,它们在周期表中位置如图所示,若W原子的最外层电子数是内层电子总数的
,下列说法中正确的是( )
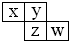
| 7 |
| 10 |
| A.阴离子的半径从大到小排列顺序为:X>Y>Z>W |
| B.X、Y两元素的氢化物分子间分别均可以形成氢键 |
| C.Y的两种同素异形体在常温下可以相互转化 |
| D.最高价氧化物对应的水化物的酸性:Z>W |
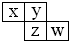
X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的
,则W原子其内层电子总数为10,最外层电子数为7,故W是Cl元素;由X、Y、Z、W在周期表中的位置关系可知,Z为S元素;Y为O元素;X为N元素.
A、核外电子排布相同,核电荷数越大,离子半径越小,所以离子半径X>Y,Z>W;最外层电子数相同,电子层越多半径越大,所以W>X,所以阴离子半径由大到小排列顺序Z>W>X>Y,故A错误;
B、X为N元素,Y为O元素,氮元素与氧元素的电负性很强,氨气与水中都存在氢键,故B正确;
C、Y为O元素,常见的两种同素异形体氧气与臭氧,空气中有大量的氧气,故二者在常温下不能相互转化,故C错误;
D、同周期元素从左到右元素的非金属性逐渐增强,所以非金属性W>Z,元素的非金属性越强,对应最高价氧化物的水化物的酸性越强,所以最高价氧化物对应水化物的酸性:W>Z,故D错误.
故选:B.
| 7 |
| 10 |
A、核外电子排布相同,核电荷数越大,离子半径越小,所以离子半径X>Y,Z>W;最外层电子数相同,电子层越多半径越大,所以W>X,所以阴离子半径由大到小排列顺序Z>W>X>Y,故A错误;
B、X为N元素,Y为O元素,氮元素与氧元素的电负性很强,氨气与水中都存在氢键,故B正确;
C、Y为O元素,常见的两种同素异形体氧气与臭氧,空气中有大量的氧气,故二者在常温下不能相互转化,故C错误;
D、同周期元素从左到右元素的非金属性逐渐增强,所以非金属性W>Z,元素的非金属性越强,对应最高价氧化物的水化物的酸性越强,所以最高价氧化物对应水化物的酸性:W>Z,故D错误.
故选:B.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
如表是元素周期表的一部分.X、Y、Z、W均为短周期元素,它们的质 子数之和为46.下列说法正确的是( )
| x | y | ||
| z | w |
| A、原子半径:W<X |
| B、气态氢化物的稳定性:Y<Z |
| C、最髙化合价:X<Y |
| D、最髙价氧化物对应的水化物的酸性:Z<W |
 如图是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和为21.下列说法正确的是( )
如图是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和为21.下列说法正确的是( )| A、X元素最多可形成六种氧化物 | B、Y元素的最高价氧化物的水化物是含氧酸中酸性最强的 | C、X元素的非金属性比Y元素非金属性强 | D、Z和X能以共价键结合形成一种无机非金属材料 |
 如图是元素周期表的一部分,X、Y、Z、W均为短周期元素,若X原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
如图是元素周期表的一部分,X、Y、Z、W均为短周期元素,若X原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )| A、元素X位于元素周期表的第二周期第ⅣA族 | B、元素W在自然界以化合态的形式存在 | C、Z的单质能在X的单质(X2)中燃烧生成ZX3 | D、元素Y的最高正化合价与元素W的相同 |
 如图为元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子的最外层电子数是其次外层电子数的
如图为元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子的最外层电子数是其次外层电子数的