题目内容
19.下列分离或提纯物质的方法正确的是( )| A. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| B. | 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 | |
| C. | 用渗析的方法精制Fe(OH)3胶体 | |
| D. | 用加热→蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
分析 A.二者均不溶于水;
B.溶液与胶体均可透过滤纸;
C.胶体不能透过半透膜,离子、分子可以;
D.CaCl2、MgCl2等蒸发时不能与NaCl分离,均为可溶性固体.
解答 解:A.二者均不溶于水,则溶解、过滤不能除杂,应加硫酸溶解后过滤,故A错误;
B.溶液与胶体均可透过滤纸,则过滤不能分离,应选渗析法,故B错误;
C.胶体不能透过半透膜,离子、分子可以,则用渗析的方法精制Fe(OH)3胶体,故C正确;
D.CaCl2、MgCl2等蒸发时不能与NaCl分离,均为可溶性固体,应加化学试剂将杂质转化为沉淀再分离,故D错误;
故选C.
点评 本题考查混合物的分离、提纯,为高频考点,把握发生的反应及混合物的分离方法、原理为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
9.下列各离子组的叙述正确的是( )
| A. | 在强酸性条件下Na+、IO-、K+、可以大量共存 | |
| B. | 在强碱性条件下K+、AlO2-、Na+、NO3-可以大量共存 | |
| C. | 在水溶液中H+、NH4+、SiO32-、Cl-不能大量共存 | |
| D. | 在强酸性条件下NH4+、K+、SO32-、S2-可以大量共存 |
10.铝热反应原理可以应用在生产上,例如焊接钢轨、冶炼难熔金属、制作传统的烟火剂等.某小组同学在研究铝热反应时,进行如下讨论和实验.
(1)关于铝热反应有以下两种认识,其中正确的是b(填字母序号).
a.该反应需在高温下发生,所以是吸热反应
b.因为铝的还原性较强,所以铝能将相对不活泼的金属从其化合物中置换出来
(2)铝和氧化铁反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+Al2O3.
(3)铝和氧化铁反应所得固体成分的初步确定.
①由上述实验可知:溶液中Fe元素的存在形式有Fe2+、Fe3+.
②i中产生H2的原因是样品中除含Fe外,可能有未反应的Al,为检验样品中是否含Al单质,可选用的试剂是NaOH溶液.
③ii中生成O2的化学方程式是2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
进一步的实验表明,上述固体样品中Fe元素的存在形式有:Fe、Fe2O3、Fe3O4.
(1)关于铝热反应有以下两种认识,其中正确的是b(填字母序号).
a.该反应需在高温下发生,所以是吸热反应
b.因为铝的还原性较强,所以铝能将相对不活泼的金属从其化合物中置换出来
(2)铝和氧化铁反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+Al2O3.
(3)铝和氧化铁反应所得固体成分的初步确定.
| 实验序号 | 操作及现象 |
| i | 取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色 |
| ii | 向i所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液,产生无色气体(经检验为O2),溶液变为深红色 |
②i中产生H2的原因是样品中除含Fe外,可能有未反应的Al,为检验样品中是否含Al单质,可选用的试剂是NaOH溶液.
③ii中生成O2的化学方程式是2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
进一步的实验表明,上述固体样品中Fe元素的存在形式有:Fe、Fe2O3、Fe3O4.
7.下列仪器使用正确的是( )
| A. | 使用漏斗、滤纸、玻璃棒等进行过滤实验 | |
| B. | 用带玻璃塞的试剂瓶盛盐酸 | |
| C. | 在表面皿蒸发浓缩NaCl溶液 | |
| D. | 配制100mL浓度为0.10 mol•L-1Na Cl溶液时,在容量瓶中溶解、定容 |
14.将一定量的Fe和Fe2O3的混合物放入250mL 1.8mol•L-1的硝酸溶液中,当固体混合物完全溶解后,在标准状况下生成1.12LNO(HNO3的还原产物仅此一种),再向反应后的溶液中加入1.0mol?L-1NaOH溶液,若要使铁元素完全沉淀,所加入的NaOH溶液的体积至少应为( )
| A. | 300mL | B. | 400mL | C. | 450mL | D. | 500mL |
4.从某海洋动物体中可以提取具有抗肿瘤的活性天然产物,实验小组按以下实验方案进行:
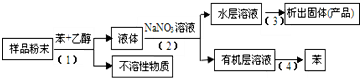
下列说法错误的是( )

下列说法错误的是( )
| A. | 步骤(3)需要用到坩埚 | B. | 步骤(2)需要用到分液漏斗 | ||
| C. | 步骤(1)需要过滤装置 | D. | 步骤(4)需要蒸馏装置 |
8.在密闭容器中进行X(g)+4Y2(g)?2Z2(g)+3Q2(g)的反应中,其中X2、Y2、Z2、Q2的开始浓度分别为0.1mol/L、0.4mol/L、0.2mol/L、0.3mol/L,当反应达到平衡后,各物质的浓度不可能是( )
| A. | c(X2)=0.15mol/L | B. | c(Y2)=0.9mol/L | C. | c(Z2)=0.3mol/L | D. | c(Q2)=0.5mol/L |
9.下列电子式书写不正确的是( )
| A. | HCl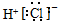 | B. | CaCl2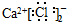 | C. | BaCl2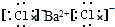 | D. | NaOH 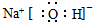 |