题目内容
高温下,某反应达到平衡,平衡常数 .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )A.升高温度,正反应速率增大,逆反应速率减小
B.该反应的焓变为正值
C.恒温恒容下,增大压强,H2浓度一定减小
D.该反应的化学方程式为CO+H2O
 CO2+H2
CO2+H2B、根据升高温度化学平衡的移动来判断反应的方向;
C、恒温恒容下,可以通过加入惰性气体来增大压强;
D、根据平衡常数表达式来确定化学方程式的表达.
解答:解:A、升高温度,正反应速率增大,逆反应速率也增大,故A错误;
B、根据平衡常数
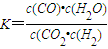 ,则反应的方程式为:CO2+H2
,则反应的方程式为:CO2+H2 CO+H2O,温度升高,H2浓度减小,说明平衡向着正向进行,所以反应是吸热反应,故B正确;
CO+H2O,温度升高,H2浓度减小,说明平衡向着正向进行,所以反应是吸热反应,故B正确;C、恒温恒容下,加入惰性气体增大压强,H2浓度不变,平衡不移动,故C错误;
D、根据平衡常数
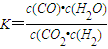 ,则反应的方程式为:CO2+H2
,则反应的方程式为:CO2+H2 CO+H2O,故D错误.
CO+H2O,故D错误.故选B.
点评:本题考查学生化学平衡常数的含义以及化学反应速率和化学平衡的移动原理知识,可以根据教材知识来回答,难度不大.

 阅读快车系列答案
阅读快车系列答案I.飞机尾气中的NO会破坏臭氧层。利用催
化剂可使尾气中的NO和CO发生反应2NO +2CO
![]() 2CO2:+N2;△H<0。已知增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积.对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中
2CO2:+N2;△H<0。已知增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积.对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中
| 实验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 1.20×10-3 | 124 | ||
| Ⅲ | 350 | 5.80×10-3 |
(1)请填全表中的各空格。
(2)请在右边给出的坐标图中,画出上表中的三
 个实验条件下混合气体中NO浓度随时间变
个实验条件下混合气体中NO浓度随时间变
化的趋势曲线图,并标明各条曲线的实验编号。
II.汽车内燃机工作时产生的高温会引起N2和O2的反应:
N2(g)+O2(g)![]() =2NO(g)是导致汽车尾气
=2NO(g)是导致汽车尾气
中含有NO的原因之一。
2000C时,向容积为2L的密闭容器中充入10molN2与5mol O2,达到平衡后NO的物质的量为2mol,则该反应的平衡常数K=___ _ 。该温度下,若开始时向上述容器中充入1 molN2和一定量的O2,平衡时O2与NO的物质的量恰好相等,则平 衡时N2的物质的量是 。
I.飞机尾气中的NO会破坏臭氧层。利用催
化剂可使尾气中的NO和CO发生反应2NO +2CO![]() 2CO2:+N2;△H<0。已知增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积.对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中
2CO2:+N2;△H<0。已知增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积.对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中
实验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
Ⅱ | 1.20×10-3 | 124 | ||
Ⅲ | 350 | 5.80×10-3 |
(1)请填全表中的各空格。
(2)请在右边给出的坐标图中,画出上表中的三
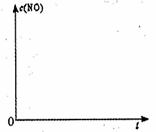 个实验条件下混合气体中NO浓度随时间变
个实验条件下混合气体中NO浓度随时间变
化的趋势曲线图,并标明各条曲线的实验编号。
II.汽车内燃机工作时产生的高温会引起N2和O2的反应:
N2(g)+O2(g)![]() =2NO(g)是导致汽车尾气中含有NO的原因之一。
=2NO(g)是导致汽车尾气中含有NO的原因之一。
2000C时,向容积为2L的密闭容器中充入10molN2与5mol O2,达到平衡后NO的物质的量为2mol,则该反应的平衡常数K=___ _ 。该温度下,若开始时向上述容器中充入1 molN2和一定量的O2,平衡时O2与NO的物质的量恰好相等,则平 衡时N2的物质的量是 。
 2H2+O2、2CO+O2
2H2+O2、2CO+O2 2H2+O2、2CO+O2
2H2+O2、2CO+O2