��Ŀ����
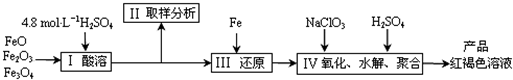
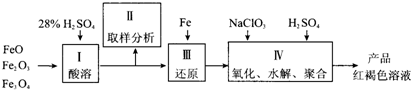
�ۺ���������PFS����һ������Ч�����߷������������㷺����ˮ�Ĵ���������һ���������������������ͼ��Ϊԭ������ȡ�ۺ���������Ϊ����ˮ��ʱFe3+��Ũ�ȣ���ֹ������������������ԭ���е�Fe3+�����Ȼ�ԭΪFe2+��ʵ�鲽�����£�

��1��ʵ������18.4 mol��L-1��Ũ������ȡ_______mL������250mL4.8 mol��L-1��������Һ�����õ��������ձ�������������Һ���⣬����Ҫ�IJ�������_____________��
��2������IIȡ��������Һ�е�Fe2+��Fe3+�ĺ�����Ŀ����_____________��
A��������Һ��Fe2+��Fe3+������
B��ȷ����һ����ԭ����������
C��ȷ������Fe2+����NaClO3����
D��ȷ������������������ȫ
��3����д�����������NaClO3����ʱ�����ӷ���ʽ____________________����ʾ��ClO3��ת��ΪCl������
����֪1mol HNO3�ļ۸�Ϊ0.16Ԫ��1mol NaClO3�ļ۸�Ϊ0.45Ԫ��������HNO3����NaClO3��Ϊ�����������ף�����__________������____________��
��4��Ϊ�˷�����Ʒ�ۺ���������Һ��SO42����Fe3+ ���ʵ���֮�ȣ�������������²���
��a��ȡ25mL�ۺ���������Һ������������BaCl2��Һ��������ɫ��������ɫ�����������ˡ�ϴ�ӡ�������أ�������Ϊm g��
��b����ȡ25mL�ۺ���������Һ����������ͭ�ۣ���ַ�Ӧ����ˡ�ϴ�ӣ�����Һ��ϴҺ�ϲ����250mL��Һ��ȡ����Һ25.00mL����KMnO4������Һ�ζ��������յ�ʱ��ȥ0.1000 mol/L KMnO4����ҺVmL�����ӷ���ʽΪ��5Fe2+ + MnO4��+ 8H+ = 5Fe3+ + Mn2+ + 4H2O
���жϣ�a��������Һ��SO42�������ѳ�����ȫ�ķ�����__________________��
���ڣ�b���������жϴﵽ�յ��������_______________��
�۾ۺ���������SO42����Fe3+�����ʵ���֮��Ϊ____________���ú�m��V�Ĵ���ʽ��ʾ����
��2������IIȡ��������Һ�е�Fe2+��Fe3+�ĺ�����Ŀ����_____________��
A��������Һ��Fe2+��Fe3+������
B��ȷ����һ����ԭ����������
C��ȷ������Fe2+����NaClO3����
D��ȷ������������������ȫ
��3����д�����������NaClO3����ʱ�����ӷ���ʽ____________________����ʾ��ClO3��ת��ΪCl������
����֪1mol HNO3�ļ۸�Ϊ0.16Ԫ��1mol NaClO3�ļ۸�Ϊ0.45Ԫ��������HNO3����NaClO3��Ϊ�����������ף�����__________������____________��
��4��Ϊ�˷�����Ʒ�ۺ���������Һ��SO42����Fe3+ ���ʵ���֮�ȣ�������������²���
��a��ȡ25mL�ۺ���������Һ������������BaCl2��Һ��������ɫ��������ɫ�����������ˡ�ϴ�ӡ�������أ�������Ϊm g��
��b����ȡ25mL�ۺ���������Һ����������ͭ�ۣ���ַ�Ӧ����ˡ�ϴ�ӣ�����Һ��ϴҺ�ϲ����250mL��Һ��ȡ����Һ25.00mL����KMnO4������Һ�ζ��������յ�ʱ��ȥ0.1000 mol/L KMnO4����ҺVmL�����ӷ���ʽΪ��5Fe2+ + MnO4��+ 8H+ = 5Fe3+ + Mn2+ + 4H2O
���жϣ�a��������Һ��SO42�������ѳ�����ȫ�ķ�����__________________��
���ڣ�b���������жϴﵽ�յ��������_______________��
�۾ۺ���������SO42����Fe3+�����ʵ���֮��Ϊ____________���ú�m��V�Ĵ���ʽ��ʾ����
��1��65.2mL��250mL����ƿ����ͷ�ι�
��2��BC
��3����6Fe2+ + ClO3�� + 6H+ = 6Fe3+ + Cl�� + 3H2O
������ԭ�ϳɱ��ϵͣ��ף���������Դ�������Ⱦ
��4����ȡ�ϲ���ҹ���μ�BaCl2��Һ������������������Һ��SO42-�ѳ�����ȫ������Һ��dz��ɫ��Ϊdz�Ϻ�ɫ���Ұ�����ڲ���ɫ����
��2��BC
��3����6Fe2+ + ClO3�� + 6H+ = 6Fe3+ + Cl�� + 3H2O
������ԭ�ϳɱ��ϵͣ��ף���������Դ�������Ⱦ
��4����ȡ�ϲ���ҹ���μ�BaCl2��Һ������������������Һ��SO42-�ѳ�����ȫ������Һ��dz��ɫ��Ϊdz�Ϻ�ɫ���Ұ�����ڲ���ɫ����


��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ

 Ҫ����;��
Ҫ����;�� ���������ؽ������ӡ���PFS������ԭ��δ�ɶԵ�����Ϊ__ ����
���������ؽ������ӡ���PFS������ԭ��δ�ɶԵ�����Ϊ__ ���� ____ ��
____ ��