题目内容
选择下列物质,填写下列空白。A.干冰 B.金刚石 C.氯化铵 D.氟化钙 ?E.固体碘 F.烧碱
(1)熔化时不需要破坏化学键的是______________(填序号,下同)。
(2)熔化时需断裂共价键的是_________________。
(3)熔点最高的是_________,熔点最低的是__________。
(4)晶体中存在分子的是__________________________。
(5)晶体中既有离子键又有共价键的是____________。
(1)AE (2)B (3)B A (4)AE (5)CF
解析:干冰为分子晶体,金刚石为原子晶体,氯化钙、氟化钙、烧碱均属于离子晶体,碘为分子晶体。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案物质 | 除杂方法(或试剂) | 化学方程式 |
CO(CO2) |
|
|
Na2CO3固体(NaHCO3) |
|
|
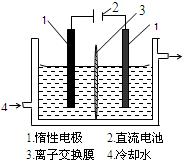
(2)某课外活动小组准备用如下图所示的装置进行实验。现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液:

| A电极 | B电极 | X溶液 |
甲 | Cu | Zn | H2SO4 |
乙 | Pt | Pt | CuCl2 |
丙 | Fe | Cu | ? |
①甲同学在实验中将电键K5闭合,Zn电极上的电极反应式为___________________________。
②乙同学准备进行电解CuCl2溶液的实验,则电解时的总反应方程式为:__________________。
实验时应闭合的电键的组合是:____________________。(从下列五项中选择所有可能组合,第三小题也在这五项中选择)
A.K1和K2 B.K1和K
③丙同学准备在Fe上镀Cu,选择了某种盐来配制电镀液,则该盐中应含的阳离子的化学式为________,实验时,应闭合的电键的组合是________(选项如上)。
![]() 碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。
碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶
于水。碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质
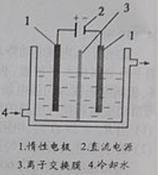
碘。以碘为原料,通过电解制备碘酸钾的实验装置如右图所示。
![]() 请回答下列问题:
请回答下列问题:
(1)碘是 (填颜色)固体物质,实验室常用
方法来分离提纯含有少量杂质的固体碘。
(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:
3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为 ;阴极上观察到的实验现象是 。
(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I—。请设计一个检验电解液中是否有I—的实验方案,并按要求填写下表。
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选。
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸。![]()
![]()
![]() w_w w. k#s5_u.c o*m
w_w w. k#s5_u.c o*m
| 实验方法 | 实验现象及结论 |
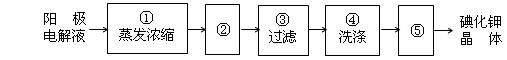
(4)电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
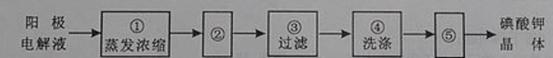
步骤②的操作名称是 ,步骤⑤的操作名称是 。步骤④洗涤晶体的目的是
。
 (2010?四川)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:
(2010?四川)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题: