题目内容
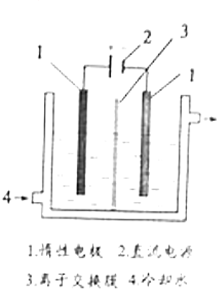 (2010?四川)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:
(2010?四川)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:(1)碘是
紫黑色
紫黑色
(填颜色)固体物质,实验室常用升华
升华
方法来分离提纯含有少量杂质的固体碘.(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:
3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区,电解槽用水冷却.电解时,阳极上发生反应的电极反应式为
2I--2e-=I2
2I--2e-=I2
;阴极上观察到的实验现象是有气泡产生
有气泡产生
.(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I-.请设计一个检验电解液中是否有I-的实验方案,并按要求填写下表.
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选.
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸.
| 实验方法 | 实验现象及结论 |
取少量阳极区电解液于试管中,加稀硫酸酸化后加入几滴淀粉溶液,观察是否变蓝. 取少量阳极区电解液于试管中,加稀硫酸酸化后加入几滴淀粉溶液,观察是否变蓝. |
如果不变蓝,说明无I-.(如果变蓝,说明有I-) 如果不变蓝,说明无I-.(如果变蓝,说明有I-) |

步骤②的操作名称是
冷却结晶
冷却结晶
,步骤⑤的操作名称是干燥
干燥
.步骤④洗涤晶体的目的是洗去吸附在碘酸钾晶体上的氢氧化钾等杂质
洗去吸附在碘酸钾晶体上的氢氧化钾等杂质
.分析:(1)碘是紫黑色固体;加热时碘易升华.
(2)阳极上阴离子放电发生氧化反应;阴极上氢离子放电发生还原反应.
(3)酸性条件下,碘离子和碘酸根离子能发生氧化还原反应生成碘单质,淀粉遇碘变蓝色,根据溶液是否变蓝判断是否含有碘离子.
(4)从热溶液中析出晶体的方法是冷却结晶;洗涤后的晶体要进行干燥;洗涤晶体的目的:洗去吸附在碘酸钾晶体上的氢氧化钾等杂质.
(2)阳极上阴离子放电发生氧化反应;阴极上氢离子放电发生还原反应.
(3)酸性条件下,碘离子和碘酸根离子能发生氧化还原反应生成碘单质,淀粉遇碘变蓝色,根据溶液是否变蓝判断是否含有碘离子.
(4)从热溶液中析出晶体的方法是冷却结晶;洗涤后的晶体要进行干燥;洗涤晶体的目的:洗去吸附在碘酸钾晶体上的氢氧化钾等杂质.
解答:解:(1)碘是紫黑色固体;加热条件下碘易升华,杂质不易升华,所以采用升华的方法分离碘单质.
故答案为:紫黑色;升华.
(2)阳极附近的阴离子有碘离子、碘酸根离子和氢氧根离子,电解过程中阳极上碘离子失电子生成碘单质,电极反应式为:2I--2e-=I2;阴极上氢离子放电生成氢气,所以阴极现象:有气泡产生.
故答案为:2I--2e-=I2;有气泡产生.
(3)电解后的溶液区含有碘酸根离子,酸性条件下,碘离子和碘酸根离子能发生氧化还原反应生成碘单质,淀粉溶液遇碘变蓝色,所以实验方法是:取少量阳极区电解液于试管中,加稀硫酸酸化后加入几滴淀粉溶液,观察是否变蓝;如果阳极区含有碘离子,加入稀硫酸后就有碘单质生成,淀粉溶液就会变蓝色,否则不变色.
故答案为:取少量阳极区电解液于试管中,加稀硫酸酸化后加入几滴淀粉溶液,观察是否变蓝;如果不变蓝,说明无I-,如果变蓝,说明有I-.
(4)从热溶液中析出晶体的方法是:冷却结晶;洗涤后的晶体有水分,所以要进行干燥;过滤后得到的晶体上吸附部分氢氧化钾等杂质,为得到较纯净的碘酸钾晶体,所以要进行洗涤.
故答案为:冷却结晶;干燥;洗去吸附在碘酸钾晶体上的氢氧化钾等杂质.
故答案为:紫黑色;升华.
(2)阳极附近的阴离子有碘离子、碘酸根离子和氢氧根离子,电解过程中阳极上碘离子失电子生成碘单质,电极反应式为:2I--2e-=I2;阴极上氢离子放电生成氢气,所以阴极现象:有气泡产生.
故答案为:2I--2e-=I2;有气泡产生.
(3)电解后的溶液区含有碘酸根离子,酸性条件下,碘离子和碘酸根离子能发生氧化还原反应生成碘单质,淀粉溶液遇碘变蓝色,所以实验方法是:取少量阳极区电解液于试管中,加稀硫酸酸化后加入几滴淀粉溶液,观察是否变蓝;如果阳极区含有碘离子,加入稀硫酸后就有碘单质生成,淀粉溶液就会变蓝色,否则不变色.
故答案为:取少量阳极区电解液于试管中,加稀硫酸酸化后加入几滴淀粉溶液,观察是否变蓝;如果不变蓝,说明无I-,如果变蓝,说明有I-.
(4)从热溶液中析出晶体的方法是:冷却结晶;洗涤后的晶体有水分,所以要进行干燥;过滤后得到的晶体上吸附部分氢氧化钾等杂质,为得到较纯净的碘酸钾晶体,所以要进行洗涤.
故答案为:冷却结晶;干燥;洗去吸附在碘酸钾晶体上的氢氧化钾等杂质.
点评:本题考查了碘的物理性质、电解原理、碘离子的检验等性质,难度不大,明确酸性条件下碘离子和碘酸根离子能生成碘单质,碱性条件下,碘能和氢氧根离子生成碘离子和碘酸根离子.

练习册系列答案
相关题目