题目内容
4.下列叙述不正确的是( )| A. | 在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 | |
| B. | 铁管上镶嵌锌块,铁管不易被腐蚀 | |
| C. | 生铁中含有碳,抗腐蚀能力比纯铁弱 | |
| D. | 将海水中的钢铁闸门与电源的负极相连,可防止闸门被腐蚀 |
分析 A.电镀时,镀层金属为阳极;
B.锌与铁形成原电池反应,锌为负极;
C.生铁中含有碳,发生发生电化学腐蚀;
D.将海水中的钢铁闸门与电源的负极相连,为外加电源的阴极保护法.
解答 解:A.电镀时,镀层金属为阳极,待镀金属为阴极,含有镀层金属离子的电解质为溶液,则在铁制品上镀铜时,镀件为阴极,铜盐为电镀液,故A错误;
B.锌与铁形成原电池反应,锌为负极,负极发生氧化反应,铁被保护,故B正确;
C.生铁中含有碳,易发生电化学腐蚀,则生铁抗腐蚀能力比纯铁弱,故C正确;
D.将海水中的钢铁闸门与电源的负极相连,铁为阴极,不易被氧化,为外加电源的阴极保护法,故D正确.
故选A.
点评 本题考查原电池和电解池原理的应用,明确电极上得失电子是解本题关键,注意把握金属的腐蚀和防护原理,题目难度不大.

练习册系列答案
相关题目
9.下列溶液中的c(Cl-)与50mL 1mol•L-1 AlCl3溶液中c(Cl-)相等的是( )
| A. | 150mL 1mol•L-1 NaCl溶液 | B. | 75mL 2mol•L-1 NH4Cl溶液 | ||
| C. | 50mL 3mol•L-1KClO3溶液 | D. | 50mL 1mol•L-1 FeCl3溶液 |
10.下列不属于配合物的是( )
| A. | [Cu(NH3)4]SO4•H2O | B. | [Ag(NH3)2]OH | C. | NH4NO3 | D. | Na[Al(OH)4] |
12.下列有关酒精的叙述错误的是( )
| A. | 易溶于水 | B. | 易挥发 | C. | 常用作有机溶剂 | D. | 不能燃烧 |
19.某溶液中有NH4+、Mg2+、Fe2+和Fe3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中下列阳离子的物质的量基本不变的是( )
| A. | NH4+ | B. | Mg2+ | C. | Fe2+ | D. | Fe3+ |
9.现有一瓶A和B的混合液,已知A和B的某些性质如下:
由此,分离A和B的最佳方法是( )
| 物质 | 熔点℃ | 沸点℃ | 密度g•cm-3 | 水溶性 |
| A | -98 | 57.5 | 0.93 | 可溶 |
| B | -84 | 97 | 0.90 | 可溶 |
| A. | 萃取 | B. | 升华 | C. | 分馏 | D. | 分液 |
16.已知同一碳原子连有两个羟基不稳定: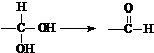
有机物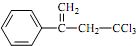 是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快.下列有关该有机物的说法正确的是( )
是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快.下列有关该有机物的说法正确的是( )
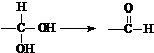
有机物
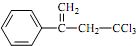 是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快.下列有关该有机物的说法正确的是( )
是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快.下列有关该有机物的说法正确的是( )| A. | 属于卤代烃,不能使酸性高锰酸钾溶液和溴水褪色 | |
| B. | 该物质存在顺反异构 | |
| C. | 在碱性条件下充分水解,可生成羧酸盐 | |
| D. | 1mol 该物质在一定条件下可与 3molH2发生加成反应 |
13.某有机物 X 的结构简式如图所示,则下列有关说法中正确的是( )


| A. | X的分子式为 C12H16O3 | |
| B. | X在核磁共振氢谱图中共出现8组峰 | |
| C. | X在一定条件下能发生加成、加聚、取代、氧化等反应 | |
| D. | 在Ni作催化剂的条件下,1mol X 最多只能与5molH2加成 |
14.下列说法正确的是( )
| A. | 戊烷、戊醇、戊烯、乙酸乙酯中同分异构体数目最少的是戊烯 | |
| B. | 分子式为C4H9Cl的有机化合物有4种 | |
| C. | 丙烯与HCl在一定条件下的产物只有一种 | |
| D. | 用CH2(NH2)-COOH和CH3-CH(NH2)-COOH两种氨基酸脱水,最多可以生成3种2肽 |