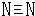题目内容
17.下列各对物质,化学键完全相同的是( )①NaCl和NaOH ②Cl2和N2 ③Na2S和(NH4)2S④SiO2和CO2⑤晶体硅和水晶.
| A. | ①②③ | B. | ② | C. | ②④ | D. | ②④⑤ |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,铵根离子和酸根离子之间存在离子键,同种非金属元素之间形成非极性共价键,不同非金属元素之间易形成极性共价键,据此分析解答.
解答 解:①NaCl中只存在离子键,NaOH中存在离子键和共价键,所以化学键不同,故不选;
②Cl2和N2中都只含极性共价键,所以化学键相同,故选;
③Na2S和(NH4)2S中,前者只含离子键,后者含有共价键和离子键,所以化学键不同,故不选;
④SiO2和CO2中,二者都只含极性共价键,所以化学键相同,故选;
⑤晶体硅和水晶中,二者都只含共价键,但前者为非极性键,后者为极性键,所以化学键不同,故不选;
故选C.
点评 本题考查化学键,为高频考点,侧重考查基本概念,明确物质构成微粒及微粒之间作用力是解本题关键,注意不能根据是否含有金属元素判断离子键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列关于氢键说法不正确的是( )
| A. | 常温时水呈液态是因为水分子间可以形成氢键 | |
| B. | NH3易溶于水的原因之一是它与水分子间能形成氢键因为能形成氢键 | |
| C. | H2O比H2S稳定是因为水分子间可以形成氢键,而H2S不能 | |
| D. | 乙醇可以与水互溶是因为它与水分子间可以形成氢键 |
5.可逆反应:2A+2B?C+3D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是( )
| A. | v(A)=0.0075 mol•L-1•min-1 | B. | v(B)=0.01 mol•L-1•mim-1 | ||
| C. | v(C)=0.5 mol•L-1•s-1 | D. | v(D)=0.4 mol•L-1•s-1 |
9.对于反应中的能量变化,表述正确的是( )
| A. | 氧化反应均为吸热反应 | |
| B. | 断开化学键的过程会放出能量 | |
| C. | 加热才能发生的反应一定是吸热反应 | |
| D. | 放热反应中,反应物的总能量大于生成物的总能量 |
6.下列说法错误的是( )
| A. | HF可以用于刻蚀玻璃 | |
| B. | 用小苏打(NaHCO3)发酵面团制作馒头 | |
| C. | SO2具有漂白性,可用于漂白纸浆,也可以大量用于漂白食品 | |
| D. | 纯碱用于生产普通玻璃,也可用纯碱溶液来除去物品表面的油污 |
7.纳米MgO可用尿素与氯化镁合成.某小组研究该反应在温度为378~398K时的反应时间、反应物配比等因素对其产率的影响.请完成以下实验设计表:
| 编号 | 温度/K | 反应时间/h | 反应物物质的量配比 | 实验目的 |
| ① | 378 | 3 | 3:1 | 实验②和④探究温度对产率的影响 实验②和③探究反应时间对产率的影响 |
| ② | 378 | 4 | 4:1 | |
| ③ | 378 | 3 | 4:1 | |
| ④ | 398 | 4 | 4:1 |
 (I)由短周期元素构成的A~E五种物质中都含有同一种元素,B为单质.
(I)由短周期元素构成的A~E五种物质中都含有同一种元素,B为单质. ,A既能与强酸又能与强碱反应,且都能产生气体,请画出A的电子式为
,A既能与强酸又能与强碱反应,且都能产生气体,请画出A的电子式为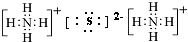 或
或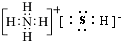 .
.