题目内容
人类的生存环境是一个巨大的生态系统,随着社会生产力的发展,环境污染已严重威胁着人类的生存环境,而森林对保护和改善环境有十分重要的作用.科学家证明1ha(公顷)柳杉林每月可吸收SO2160kg.试回答下列问题:
(1)柳杉可吸收SO2,说明森林对环境的作用是 .
(2)某火力发电厂每月燃烧含硫1%的烟煤10000t,若要吸收该厂所排出的烟道气中的SO2,至少需要柳杉林多少公顷?若该厂在排放烟道气之前用脱硫法处理,每年可回收硫多少千克?这些硫可生产98%的浓H2SO4多少千克?
(1)柳杉可吸收SO2,说明森林对环境的作用是
(2)某火力发电厂每月燃烧含硫1%的烟煤10000t,若要吸收该厂所排出的烟道气中的SO2,至少需要柳杉林多少公顷?若该厂在排放烟道气之前用脱硫法处理,每年可回收硫多少千克?这些硫可生产98%的浓H2SO4多少千克?
考点:二氧化硫的污染及治理
专题:氧族元素
分析:(1)依据“科学家证明1ha(公顷)柳杉林每月可吸收SO2160kg”解答;
(2)硫的质量=烟煤的质量×硫的百分含量;
依据硫原子个数守恒可知:S~SO2~H2SO4,据此计算产生二氧化硫的质量和硫酸的质量,依据每公顷柳杉吸收二氧化硫160g,计算出吸收该厂所排出的烟道气中的SO2需要柳杉林的公顷;
(2)硫的质量=烟煤的质量×硫的百分含量;
依据硫原子个数守恒可知:S~SO2~H2SO4,据此计算产生二氧化硫的质量和硫酸的质量,依据每公顷柳杉吸收二氧化硫160g,计算出吸收该厂所排出的烟道气中的SO2需要柳杉林的公顷;
解答:
解:(1)二氧化硫有毒,能污染空气,柳杉可吸收SO2,起到净化空气,维护生态平衡的作用;
(2)10000t煤含S的量为=10000t×1%=100t,则转化成SO2的量为200t,每公顷柳杉吸收二氧化硫160g,所以需种植的面积200t/0.16t=1250公顷;
每年可回收硫的质量=10000t×1%×12=12×100t=1200t=1.2×106kg;
设生成98%的浓H2SO4m千克,依据原子个数守恒得:
S~SO2 ~H2SO4,
32 98
1.2×106kg m×98%
32×m×98%=98×1.2×106kg
解得m=3.75×106kg,
答:若要吸收该厂所排出的烟道气中的SO2,至少需要柳杉林1250公顷;若该厂在排放烟道气之前用脱硫法处理,每年可回收硫1.2×106kg;这些硫可生产98%的浓H2SO43.75×106kg.
(2)10000t煤含S的量为=10000t×1%=100t,则转化成SO2的量为200t,每公顷柳杉吸收二氧化硫160g,所以需种植的面积200t/0.16t=1250公顷;
每年可回收硫的质量=10000t×1%×12=12×100t=1200t=1.2×106kg;
设生成98%的浓H2SO4m千克,依据原子个数守恒得:
S~SO2 ~H2SO4,
32 98
1.2×106kg m×98%
32×m×98%=98×1.2×106kg
解得m=3.75×106kg,
答:若要吸收该厂所排出的烟道气中的SO2,至少需要柳杉林1250公顷;若该厂在排放烟道气之前用脱硫法处理,每年可回收硫1.2×106kg;这些硫可生产98%的浓H2SO43.75×106kg.
点评:本题考查了二氧化硫的污染和治理,以及相关计算,侧重考查学生根据材料分析问题、解决问题的能力,培养学生保护森林,树立环保的意识,相关计算是本题的难点,注意依据原子个数守恒解答,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为l:2,下列有关该有机物分子组成的推论正确的是( )
| A、分子中C、H、O个数之比为1:4:4 |
| B、分子中C、H个数之比为1:2 |
| C、分子中可能含有氧原子 |
| D、此有机物的最简式为CH4 |
有关物质的量浓度溶液配制的下列说法中正确的是( )
| A、将1mol NaCl溶于1L水中所得溶液物质的量浓度为1mol?L-1 |
| B、将0.1mol NaCl投入100mL容量瓶中加水至刻度线,充分振荡后浓度为1 mol?L-1 |
| C、称取4.0g NaOH放入烧杯中并加水搅拌后立即全部转移到容量瓶中定容 |
| D、需要48mL 0.1 mol?L-1的Na2CO3溶液,配制时应选用50mL容量瓶 |
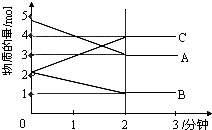 (1)写出该密闭容器发生反应的化学方程式为
(1)写出该密闭容器发生反应的化学方程式为