题目内容
已知:CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都属于离子型化合物;碳化钙(CaC2)和水发生反应制备C2H2的方程式如下:CaC2+2H2O→C2H2↑+Ca(OH)2.请通过CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是( )
| A、ZnC2水解生成乙烷(C2H6) |
| B、Al4C3水解生成丙烷(C3H4) |
| C、Mg2C3水解生成丙炔(C3H4) |
| D、Li2C2水解生成乙烯(C2H4) |
考点:乙炔炔烃
专题:类比迁移思想
分析:CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等同属于离子型碳化物,已知CaC2+2H2O→C2H2↑+Ca(OH)2,根据原子守恒分别写出离子型碳化物与水反应的方程式,在判断选项中产物是否正确.
解答:
解:A、ZnC2与水反应生成Zn(OH)2,根据原子守恒得:ZnC2+2H2O→Zn(OH)2+C2H2↑,所以另一种产物为C2H2,故A错误;
B、Al4C3与水反应生成Al(OH)3,根据原子守恒得:Al4C3+12H2O→4Al(OH)3+3CH4↑,所以所以另一种产物为CH4,故B错误;
C、Mg2C3与水反应生成Mg(OH)2,根据原子守恒得:Mg2C3+4H2O→2Mg(OH)2+C3H4↑,所以另一种产物为C3H4,故C正确;
D、Li2C2与水反应生成Zn(OH)2,根据原子守恒得:Li2C2+2H2O→2LiOH+C2H2↑,所以另一种产物为C2H2,故D错误;
故选C.
B、Al4C3与水反应生成Al(OH)3,根据原子守恒得:Al4C3+12H2O→4Al(OH)3+3CH4↑,所以所以另一种产物为CH4,故B错误;
C、Mg2C3与水反应生成Mg(OH)2,根据原子守恒得:Mg2C3+4H2O→2Mg(OH)2+C3H4↑,所以另一种产物为C3H4,故C正确;
D、Li2C2与水反应生成Zn(OH)2,根据原子守恒得:Li2C2+2H2O→2LiOH+C2H2↑,所以另一种产物为C2H2,故D错误;
故选C.
点评:本题考查了离子型碳化物的水解反应,注意类比迁移思想的应用和原子守恒的应用,题目较简单.

练习册系列答案
相关题目
下列有关化学实验操作正确的是( )
A、 称取NaOH固体 |
B、 稀释浓H2SO4 |
C、 将乙醇与水分离 |
D、 检查装置的气密性 |
最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”--全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划.有关全氟丙烷的说法不正确的是( )
| A、分子中三个碳原子不可能处于同一直线上 |
| B、相同压强下,沸点:C3F8>C3H8 |
C、全氟丙烷的电子式为: |
| D、全氟丙烷分子中既有极性键又有非极性键 |
一定浓度的下列溶液,不外加任何试剂,就能依次鉴别出来的先后顺序是( )
①NaOH溶液 ②MgSO4溶液 ③BaCl2溶液 ④KNO3溶液 ⑤FeCl3溶液.
①NaOH溶液 ②MgSO4溶液 ③BaCl2溶液 ④KNO3溶液 ⑤FeCl3溶液.
| A、①②③④⑤ |
| B、②③⑤④① |
| C、⑤①②③④ |
| D、⑤③②①④ |
下列各图所示的实验原理、方法、装置或操作正确的是( )
A、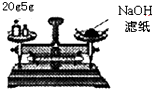 称取固体质量 |
B、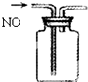 收集NO气体 |
C、 配制溶液 |
D、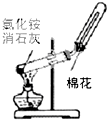 制取氨 |
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①③相连时,③有气泡逸出;①②相连时,外电路电子从②流向①;③④相连时,③的质量减少,据此判断这四种金属活动性由大到小的顺序是( )
| A、①③②④ | B、①③④② |
| C、②①③④ | D、③①②④ |
在一定温度和压强下,将一个容积为15mL的试管充满NO2后,倒置于一个盛水的水槽中,当试管内液面上升至一定高度不再变化时,相同条件下再通入O2,若要使试管内液面仍保持在原高度,则应通入O2体积为( )
| A、3.75 mL |
| B、7.5 mL |
| C、8.75 mL |
| D、10.5 mL |
 1,2二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.189.cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可用下列反应制备1,2二溴乙烷.
1,2二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.189.cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可用下列反应制备1,2二溴乙烷.