题目内容
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑,对于该反应,下列判断错误的是( )
| A、该反应能在瞬间完成,并产生大量气体 |
| B、若有1molKNO3参加反应,转移电子的物质的量为10 mol |
| C、该反应中的还原剂为NaN3 |
| D、被氧化和被还原的N原子的物质的量之比为15:1 |
考点:氧化还原反应
专题:
分析:该反应中N元素化合价由-
价、+5价变为0价,所以叠氮化钠属于还原剂、硝酸钾属于氧化剂,氧化剂被还原、还原剂被氧化,据此分析解答.
| 1 |
| 3 |
解答:
解:该反应中N元素化合价由-
价、+5价变为0价,所以叠氮化钠属于还原剂、硝酸钾属于氧化剂,
A.该反应中反应物没有气体、生成物有气体,且反应剧烈并产生大量气体,故A正确;
B.若有1molKNO3参加反应,转移电子的物质的量=1mol×(5-0)=5 mol,故B错误;
C.该反应中叠氮化钠中N元素化合价由-
价变为0价,所以叠氮化钠属于还原剂,故C正确;
D.根据方程式知,叠氮化钠是还原剂、硝酸钾是氧化剂,还原剂和氧化剂的物质的量之比为10:2=5:1,一个叠氮化钠中含有3个N原子,所以被氧化和被还原的N原子的物质的量之比为15:1,故D正确;
故选B.
| 1 |
| 3 |
A.该反应中反应物没有气体、生成物有气体,且反应剧烈并产生大量气体,故A正确;
B.若有1molKNO3参加反应,转移电子的物质的量=1mol×(5-0)=5 mol,故B错误;
C.该反应中叠氮化钠中N元素化合价由-
| 1 |
| 3 |
D.根据方程式知,叠氮化钠是还原剂、硝酸钾是氧化剂,还原剂和氧化剂的物质的量之比为10:2=5:1,一个叠氮化钠中含有3个N原子,所以被氧化和被还原的N原子的物质的量之比为15:1,故D正确;
故选B.
点评:本题考查氧化还原反应,侧重考查基本概念、基本计算,注意叠氮化钠中N元素化合价是解本题关键,题目难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
下列有关生活和生产中化学知识描述正确的是( )
| A、日常生活中使用可降解塑料以防止“白色污染” |
| B、“雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物无关 |
| C、酸雨的形成主要是因为化石燃料燃烧排放的废气中含有大量的碳氧化物 |
| D、“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 |
下列说法正确的是( )
| A、烧碱固体在水中溶解的过程是放热反应 |
| B、P2O5和CaO可以作干燥剂,利用了它们具有易潮解的性质 |
| C、FeCl3固体溶于蒸馏水可制得FeCl3溶液 |
| D、粗盐易潮解是因为其中含有CaCl2和MgCl2等杂质的缘故 |
在离子浓度都为0.1mol/L的下列溶液中,加入(或通入)某物质后,发生反应先后顺序正确的是( )
| A、在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+ |
| B、在含I-、SO32-、Br-的溶液中不断通入氯气:I-、Br-、SO32- |
| C、在含Fe3+、H+、NH4+的溶液中逐滴加入烧碱溶液:Fe3+、NH4+、H+ |
| D、在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32- |
制备单质硅时,主要化学反应如下:①SiO2+2C
Si+2CO↑ ②Si+2Cl
SiCl4 ③SiCl4+H2
Si+4HCl下列对上述三个反应的叙述中,不正确的是( )
| ||
| ||
| ||
| A、①③为置换反应 |
| B、①②③均为氧化还原反应 |
| C、②为化合反应 |
| D、三个反应的反应物中硅元素均被氧化 |
下列表达中不正确的是( )
| A、1molH2 |
| B、2molNa2CO3 |
| C、2molOH- |
| D、0.5mol氧 |
YBa2Cu8Ox(Y为元素钇)是磁悬浮列车中的超导材料,关于
Y的说法不正确的是( )
89 39 |
A、
| ||||
| B、质子数与中子数之差为50 | ||||
| C、原子的核外电子数是39 | ||||
D、
|
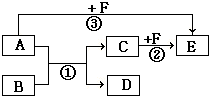 有A、B、C、D、E、F六种物质,它们之间相互转化的关系如图所示(反应条件及部分产物未标出).
有A、B、C、D、E、F六种物质,它们之间相互转化的关系如图所示(反应条件及部分产物未标出).