题目内容
在一定温度下,反应A2(g)+B2(g) 2AB(g) 达到反应限度的标志是( )
2AB(g) 达到反应限度的标志是( )
 2AB(g) 达到反应限度的标志是( )
2AB(g) 达到反应限度的标志是( )分析:根据化学平衡状态的定义,明确化学平衡状态判断标准,对选项进行判断.
解答:解:A:可逆反应是动态平衡,到达平衡时,速率不为零,正、逆反应速率相等(指同一物质的生成速率等于其消耗速率),只是外在的宏观表现不变.故A错
B:可逆反应到达平衡时,反应混合物各组分的浓度保持不变,浓度之比并不一定等于化学计量数之比,故B错
C:反应混合物各组分的物质的量不再改变,说明可逆反应到达平衡,故C对
D:从反应开始到达平衡状态,消耗nmolA2的同时一定生成2nmolAB,不能说明达到平衡状态,故D错
故选C
B:可逆反应到达平衡时,反应混合物各组分的浓度保持不变,浓度之比并不一定等于化学计量数之比,故B错
C:反应混合物各组分的物质的量不再改变,说明可逆反应到达平衡,故C对
D:从反应开始到达平衡状态,消耗nmolA2的同时一定生成2nmolAB,不能说明达到平衡状态,故D错
故选C
点评:考查对化学平衡概念的理解,选择某一标准判断可逆反应是否到达平衡状态,选择的标准应该是随反应进行是变化的,该标准由变化到不变,说明到达平衡状态,不能选择自始至终不变化的.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
将1mol A(g)和2mol B(g)置于2L某密闭容器中,在一定温度下发生反应:A(g)+2B(g)?C(g)+D(g)△H<0,C的体积分数随时间变化如图l中曲线a所示 下列说法正确的是( )
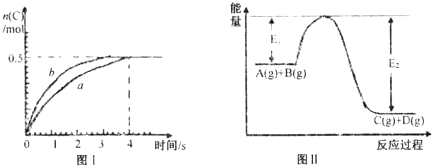

| A、此反应过程中的能量变化可用上图II表示 | B、此温度下,该反应的平衡常数的值为1 | C、该反应4s内平均速率v(A)=0.125mol?L-1?s-1 | D、若在恒温加大反应容器的容积条件下,该反应将按b曲线进行 |
