题目内容
将铁片和银片用导线连接置于同一稀盐酸中,经过一段时间后,下列叙述正确的是
| A.负极有Cl2逸出,正极有H2逸出 | B.负极附近Cl-的浓度逐渐减小 |
| C.正极附近Cl-的浓度逐渐增大 | D.溶液中Cl-的浓度基本不变 |
D
解析试题分析:铁片-银片-稀盐酸溶液构成了原电池,较活泼的金属铁作负极,银作正极,负极上铁失电子发生氧化反应,正极上氢离子得电子发生还原反应,溶液中阳离子向正极移动,阴离子向负极移动。所以溶液中的氢离子向正极移动,正极有氢气放出。氯离子向负极移动,导致负极附近氯离子的浓度逐渐增大,但溶液中的氯离子浓度是不变的,所以选项D正确,其余选项都是错误的,答案选D。
考点:考查原电池原理的应用和有关判断
点评:该题是高考中的常见考点,试题紧扣教材,基础性强,侧重对学生基础知识的巩固和检验。明确正负极上发生的电极反应、溶液中离子的移动方向即可解答本题,有利于培养学生的逻辑思维能力和灵活应变能力。

练习册系列答案
相关题目
按下图装置进行实验,下列描述正确的是(N装置中两个电极均为石墨棒)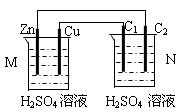
| A.C1上发生还原反应 |
| B.M 装置中SO42-移向Cu电极 |
| C.工作一段时间后装置M 中溶液pH变大,装置N中溶液pH变小 |
| D.Cu电极与C2电极上的电极反应相同 |
我国知名企业比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其它材料电池,电池总反应为:V2O5+xLi LixV2O5。下列说法正确的是
LixV2O5。下列说法正确的是
| A.该电池充电时,锂极与外电源的负极相连 |
| B.电池在放电时,Li+向负极移动 |
| C.该电池充电时阴极的反应为:LixV2O5 -xe-=V2O5 + xLi+ |
| D.若放电时转移0.2 mol 电子,则用去的锂为1.4 x g |
中国在2009年推出了国产燃料电池概念汽车,该车装有“绿色心脏”——质子交换膜燃料电池.如图是某科技杂志登载的该电池原理示意图.下列叙述正确的是( )
| A.工作时“X极”周围溶液的酸性增强 |
| B.氢气在电极上发生还原反应 |
| C.图中标出的“Y极”实际是原电池的负极 |
| D.工作过程中,质子(H+)从“Y极”一边透过质子交换膜移动到“X极”一边与OH-反应生成水 |
关于下图所示的原电池,下列说法正确的是 
| A.电子从锌电极通过电流表流向铜电极 |
| B.盐桥中的阴离子向硫酸铜溶液中迁移 |
| C.取出盐桥后,电流计的指针仍发生偏转 |
| D.铜电极上发生的电极反应是2H+ + 2e- = H2↑ |
有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
| 实验装置 |  |  |  |  |
| 部分实验现象 | a极质量减小 b极质量增加 | b极有气体产生 c极无变化 | d极溶解 c极有气体产生 | 电流计指示在导线中 电流从a极流向d极 |
A.a>b>c>d B.b>c>d>a C.d>a>b>c D.a>b>d>c
下列有关电池叙述不正确的是( )
| A.锌锰干电池是一种常用的二次电池 |
| B.氢氧燃料电池比火力发电的能量转变率要高 |
| C.锌锰干电池工作一段时间后锌外壳逐渐变薄 |
| D.碱性燃料电池正极反应是O2 + 2H2O + 4e- =4OH- |
