题目内容
12.下列有关仪器的使用正确的是( )| A. | 做金属钠与水反应实验时,剩余的钠不能再放入原试剂瓶 | |
| B. | 配制480mLNaOH溶液需要的主要仪器有480mL容量瓶、玻璃棒、烧杯、量筒等 | |
| C. | 将固体药品放在蒸发皿中进行高温焙烧 | |
| D. | 冷凝管中冷却水的流向一定是下口进水、上口出水 |
分析 A.对化学实验剩余药品,大多是不可以放回原瓶的,但是极少数例外,如金属钠切下一小块后可放回原瓶;
B.容量瓶只有一个刻度;
C.蒸发皿不能焙烧固体;
D.冷凝水下进上出.
解答 解:A.从试剂瓶中取出并切下使用的钠块后,剩余的钠要放回原试剂瓶,故A错误;
B.实验室中没有480mL容量瓶,应改用500mL的,故B错误;
C.焙烧固体应放在坩埚中进行,故C错误;
D.为加强冷凝效果冷却水的流向就应是“下进上出”,故D正确.
故选D.
点评 本题考查常见仪器的使用和化学基本操作的方法,为高频考点,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
相关题目
2. 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
请回答下列问题:
(1)上述反应的化学平衡常数表达式为$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$.该反应的Q<0(填“>”或“<”).
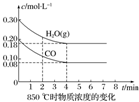
(2)850℃时在体积为10L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的物质的量浓度变化如图所示,则0~4min时平均反应速率v(CO)=0.03mol/(L•min).
(3)若在500℃时进行.且CO、H2O(g)的起始浓度均为0.020mol•L-1,该条件下,CO的最大转化率为75%.
(4)若在850℃时进行,设起始时CO和H2O(g)共为1mol,其中H2O(g)的体积分数为x,平衡时CO的转化率为y,试推导y与x之间的关系x=y.
 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
(1)上述反应的化学平衡常数表达式为$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$.该反应的Q<0(填“>”或“<”).
(2)850℃时在体积为10L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的物质的量浓度变化如图所示,则0~4min时平均反应速率v(CO)=0.03mol/(L•min).
(3)若在500℃时进行.且CO、H2O(g)的起始浓度均为0.020mol•L-1,该条件下,CO的最大转化率为75%.
(4)若在850℃时进行,设起始时CO和H2O(g)共为1mol,其中H2O(g)的体积分数为x,平衡时CO的转化率为y,试推导y与x之间的关系x=y.
20.某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等.为确定该溶液X的成分,某学习小组做了如图实验,则下列说法正确的是( )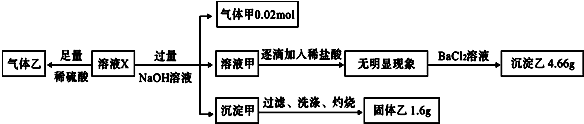

| A. | 气体甲、沉淀甲一定为纯净物 | |
| B. | CO32-、Al3+、K+一定不存在 | |
| C. | SO42-、NH4+一定存在,NO3-、Cl-可能不存在 | |
| D. | 若含有Fe3+,则一定含有Cl- |
17.下列有关离子方程式与所述事实相符且正确的是( )
| A. | Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++2OH-+2H++SO${\;}_{4}^{2-}$═BaSO4↓+2H2O | |
| B. | 用氯化铁溶液和沸水反应制取氢氧化铁胶体:Fe3++3H2O(沸水)═Fe(OH)3↓+3H+ | |
| C. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | 澄清石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H20 |
4.25℃时,下列溶液中微粒间的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1(NH4)2SO4溶液:(NH4+)>c(S042-)>c(H+)>(0H-) | |
| B. | 浓度均为0.1 mol•L-1的Na2CO3和NaHCO3等体积混合后的溶液:(Na+)>c(CO32-)>c(HCO3-)>(0H-) | |
| C. | 浓度均为0.1 mol•L-1NH3•H2O和NH4Cl等体积混合后的溶液:c(Cl-)>c(NH4+)>c(NH3•H2O) | |
| D. | 0.1 mol•L-1(Na)2S溶液:(0H-)=c(H+)+c(HS-)+c(H2S) |
7.相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是( )
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
| A. | N2的转化率:②>①>③ | B. | 三个容器内反应的平衡常数:③>①>② | ||
| C. | 平衡时氨气的体积分数:①>③ | D. | 放出热量关系:2a<c<184.8 kJ |
8.在下列反应中,HCl既表现酸性又表现氧化性的是( )
| A. | CaCO3+2HCl=CaCl2+H2O+CO2↑ | |
| B. | Fe+2HCl═FeCl2+H2↑ | |
| C. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑ | |
| D. | NaOH+HCl=NaCl+H2O |