题目内容
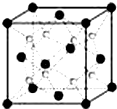
如图所示的Cu-Zn原电池,下列叙述正确的是( )


| A、氢离子在负极得电子 |
| B、锌为负极,发生氧化反应 |
| C、铜为负极,铜片上有气泡产生 |
| D、电子从铜极流向锌极 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该原电池中,Zn易失电子作负极、Cu作正极,负极反应为Zn-2e-=Zn2+、正极反应为2H++2e-=H2↑,电子从负极沿导线流向正极,据此分析解答.
解答:
解:该原电池中,Zn易失电子作负极、Cu作正极,负极反应为Zn-2e-=Zn2+、正极反应为2H++2e-=H2↑,
A.氢离子在正极上得电子发生还原反应,故A错误;
B.锌易失电子发生氧化反应而作负极,故B正确;
C.铜为正极,正极反应为2H++2e-=H2↑,所以铜电极上有气泡生成,故C错误;
D.电子从负极Zn流向正极Cu,故D错误;
故选B.
A.氢离子在正极上得电子发生还原反应,故A错误;
B.锌易失电子发生氧化反应而作负极,故B正确;
C.铜为正极,正极反应为2H++2e-=H2↑,所以铜电极上有气泡生成,故C错误;
D.电子从负极Zn流向正极Cu,故D错误;
故选B.
点评:本题考查了原电池原理,根据失电子难易程度确定正负极,再结合正负极上发生的反应分析解答,题目难度不大.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
实验室保存下列药品的方法不正确的是( )
| A、氢氟酸保存在密封的玻璃瓶中 |
| B、氢氧化钠溶液保存在带橡皮塞的试剂瓶中 |
| C、少量金属钠保存在煤油中 |
| D、硅酸钠保存在带橡皮塞的试剂瓶中 |
2.3g钠投入100g水中,下列叙述述错误的是( )
| A、钠浮在水面,熔化成银色光亮的小球 |
| B、钠贮存在煤油中 |
| C、所得溶液的质量分数为2.25% |
| D、反应中转移0.1mol电子 |
已知2SO2(g)+O2(g)?2SO3(g) (正反应放热).若在500℃和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法不正确的是( )
| A、若降低温度,可以减慢反应速率 |
| B、催化剂既能加快化学反应速率,又能提高SO2的转化率 |
| C、氧气足量时,SO2不能完全转化为SO3 |
| D、达到平衡时,SO2和SO3的浓度一定相等 |
关于原子或离子结构的下列说法不正确的是( )
| A、某原子K层上只有一个电子 |
| B、某原子M层上电子数为L层上电子数的4倍 |
| C、某离子M层上和L层上的电子数均为K层的4倍 |
| D、某离子核电荷数与最外层电子数相等 |
某溶液中含有HCO3-、SO32-、CO32-、Cl-四种阴离子.向其中加入足量的Na2O2固体后,溶液中离子浓度保持不变的是(假设溶液体积无变化)( )
| A、HCO3- |
| B、SO32- |
| C、CO32- |
| D、Cl- |
下列说法不正确的是( )
| A、体系有序性越高,熵值就越低 |
| B、自发过程将导致体系的熵增大 |
| C、吸热反应不可以自发进行 |
| D、同种物质气态时熵值最大 |
下列物质发生变化时,所克服的粒子间相互作用属同种类型的是( )
| A、碘与干冰分别受热变为气体 |
| B、硝酸铵与硝酸分别受热变为气体 |
| C、氯化钠与氯化氢分别溶解在水中 |
| D、二氧化硅晶体与冰分别受热熔化 |
 A~G是前四周期原子序数依次增大的七种元素.A、C的价电子层中未成对电子数都是2;D+与C的简单离子具有相同离子结构;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G为周期表第11列元素.回答下列问题:
A~G是前四周期原子序数依次增大的七种元素.A、C的价电子层中未成对电子数都是2;D+与C的简单离子具有相同离子结构;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G为周期表第11列元素.回答下列问题: