题目内容
键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。参考以下表格的键能数据,回答下列问题:
|
化学键 |
Si—O |
Si—Cl |
H—H |
H—Cl |
Si—Si |
Si—C |
|
键能/kJ·mol-1 |
460 |
360 |
436 |
431 |
176 |
347 |
(1)比较下列两组物质的熔点高低(填“>”或“<”)
SiC__________Si; SiCl4___________SiO2
(2)能不能根据键能的数据判断单质Si 和化合物SiCl4的熔点高低?____________(填“能”或“不能”),理由是___________________(提示对比二者晶体类型及内部微粒作用力)
(3)如右图立方体中心的“·”表示金刚石晶体中的一个原子,请在立方体的顶点用“·”表示出与之紧邻的碳原子;

(4)工业上高纯硅可通过下列反应制取:
SiCl4(g) + 2H2(g) 高温 Si(s)+4HCl(g)
计算该反应的反应热△H为______________________(要包含数据和焓变单位)
(1)SiC>Si; SiCl4<SiO2
(2) 不能 ;理由: 二者所属晶体类型不同,微粒间作用力不同,不能简单用键能比较熔点高低
(3)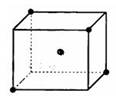 (4) +236kJ/mol
(4) +236kJ/mol
【解析】(1)碳化硅和硅形成的晶体是原子晶体,其熔点大小和晶体中共价键的强弱有关系。由于碳原子的半径小于硅原子的,所以碳化硅中共价键要其余硅中额共价键,即碳化硅的熔点高于硅的。四氯化硅是分子晶体,二氧化硅和原子晶体,所以熔点是二氧化硅的高。
(2)根据(1)中分析可知,二者所属晶体类型不同,微粒间作用力不同,不能简单用键能比较熔点高低。
(3)金刚石晶体中,每1个碳原子以4个共价单键对称地与相邻的4个碳原子结合,形成正四面体,所以结构如图所示。
(4)反应热就是断键吸收的能量和形成化学键所放出的能量的差值,即360kJ/mol×4+2×436kJ/mol-2×176kJ/mol-4×431kJ/mol=+236kJ/mol。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案 有A、B、C、D、E、F六种元素,已知:它们位于三个不同短周期,核电荷数依次增大;A与E、B与F分别同主族;A、E分别都能与D按原子个数比1﹕1或2﹕l形成化合物;B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物.
有A、B、C、D、E、F六种元素,已知:它们位于三个不同短周期,核电荷数依次增大;A与E、B与F分别同主族;A、E分别都能与D按原子个数比1﹕1或2﹕l形成化合物;B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物.
 键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.参考以下表格的键能数据,回答下列问题:
键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.参考以下表格的键能数据,回答下列问题: