题目内容
已知H2(g)+Br2(l)=2HBr(g) △H=—72 kJ/mol,蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
|
|
H2(g) |
Br2(g) |
HBr(g) |
|
1mol分子中的化学键断裂时需要吸收的能量/kJ |
436 |
a |
369 |
则下列说法正确的是( )
A.Br2(l)=Br2(g) △S<0
B.Br2(l)=Br2(g) △H=—30 kJ/mol
C.H-H键的键能为436 kJ
D.a=200
【答案】
D
【解析】
试题分析:A项Br2(l)=Br2(g),混乱度增大,△S>0;B项Br2(l)=Br2(g)是吸热反应,△H=+30 kJ/mol;C项H-H键的键能为436 kJ/mol;D项根据键能计算:369×2-436-a-30=72,求出a=200,正确。
考点:考查热化学方程式的含义及键能的计算。
点评:根据反应热等于反应物的键能减去生成物的键能,本题难度不大。

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
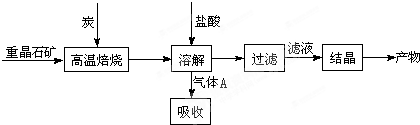
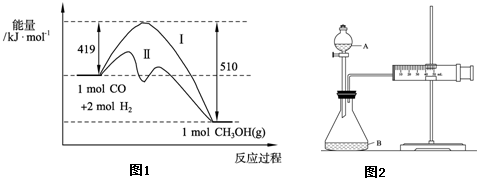


 (mol·L-1·min-1)
(mol·L-1·min-1) 减小
减小