题目内容
下列说法正确的是( )
| A、碘是人体必需的微量元素,所以要多吃含I2的食盐 |
| B、半导体材料是含硅化合物 |
| C、熔化烧碱可选用瓷坩埚 |
| D、正长石KAlSi3O8用氧化物形式可表示为K2O?Al2O3?6SiO2 |
考点:碘与人体健康,硅和二氧化硅,硅的用途
专题:
分析:A、人体补碘,不是碘单质,是元素,碘单质对人有害;
B、硅是半导体材料;
C、用石英坩埚熔化烧碱,易炸裂;
D、根据硅酸盐的氧化物表示方法来书写.
B、硅是半导体材料;
C、用石英坩埚熔化烧碱,易炸裂;
D、根据硅酸盐的氧化物表示方法来书写.
解答:
解:A、碘单质对人有害,补碘指的是碘元素,如碘酸钾,不是碘单质,故A错误;
B、硅单质是半导体材料,故B错误;
C、在加热条件下,二氧化硅与氢氧化钠反应,用石英坩埚熔化烧碱,易炸裂,故C错误;
D、硅酸盐的氧化物表示方法:先写活泼金属氧化物,然后是不活泼的金属氧化物,再是非金属氧化物二氧化硅,最后是水,所以斜长石的氧化物形式可表示为:K2O?Al2O3?6SiO2,故D正确,
故选D.
B、硅单质是半导体材料,故B错误;
C、在加热条件下,二氧化硅与氢氧化钠反应,用石英坩埚熔化烧碱,易炸裂,故C错误;
D、硅酸盐的氧化物表示方法:先写活泼金属氧化物,然后是不活泼的金属氧化物,再是非金属氧化物二氧化硅,最后是水,所以斜长石的氧化物形式可表示为:K2O?Al2O3?6SiO2,故D正确,
故选D.
点评:本题考查常见实验仪器的结构与使用方法、物质的保存等知识,难度不大,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
相关题目
已知:2H2O2=O2↑+2H2O,下列各组实验中,反应速率最快的是( )
| 实验序号 | H2O2溶液浓度/% | H2O2溶液体积/mL | 温度/℃ | MnO2用量/g |
| A | 5 | 10 | 20 | 0.1 |
| B | 15 | 10 | 20 | 0.1 |
| C | 20 | 10 | 30 | 0 |
| D | 20 | 10 | 30 | 0.1 |
| A、A | B、B | C、C | D、D |
2011年11月1日凌晨,“神舟八号”飞船成功发射升空,开启了与“天宫一号”交会对接之旅.宇宙飞船用镍钛合金制成自展天线,能在低温下被折叠,在阳光照射下可重新展开,关于此天线制作材料的描述错误的是( )
| A、具有形状记忆功能 |
| B、具有很低的熔点 |
| C、具有良好的延展性 |
| D、具有良好的导电性 |
某溶液中有Mg2+﹑Fe2+﹑Fe3+和Al3+四种阳离子,若向其中加入过量的NaOH溶液,微热并搅拌,过滤,在滤渣中再加入过量的盐酸,所得溶液中大量减少的阳离子是( )
| A、Mg2+ |
| B、Fe2+ |
| C、Fe3+ |
| D、Al3+ |
下列有关盐酸的说法中正确的是( )
| A、纯净的盐酸是纯净物 |
| B、盐酸就是液态氯化氢 |
| C、盐酸中所有阳离子所带的正电荷数与所有阴离子所带的负电荷数相等 |
| D、浓盐酸有腐蚀性,稀盐酸没有腐蚀性 |
与下列反应对应的离子方程式书写正确的是( )
| A、铁跟稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、碳酸钙溶于醋酸:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、Na2CO3溶液的水解:CO32-+2H2O?H2CO3+2OH- |
| D、碳酸镁跟硫酸反应:MgCO3+2H+=Mg2++H2O+CO2↑ |
下列各图中,表示正反应是吸热反应的图是( )
A、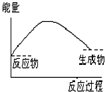 |
B、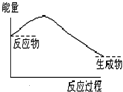 |
C、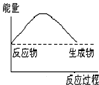 |
D、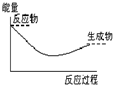 |
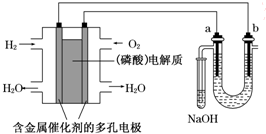 用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中,正确的是( )
用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中,正确的是( )| A、电池工作时,正极反应式为:O2+2H2O+4e-═4OH- |
| B、电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者 |
| C、电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 |
| D、忽略能量损耗,当电池中消耗0.2 g H2时,b极周围会产生2.24L H2 |
