题目内容
某溶液中有Mg2+﹑Fe2+﹑Fe3+和Al3+四种阳离子,若向其中加入过量的NaOH溶液,微热并搅拌,过滤,在滤渣中再加入过量的盐酸,所得溶液中大量减少的阳离子是( )
| A、Mg2+ |
| B、Fe2+ |
| C、Fe3+ |
| D、Al3+ |
考点:离子共存问题,离子反应发生的条件
专题:
分析:加入过量的氢氧化钠溶液,微热并搅拌,四种离子均反应,铝离子转化为偏铝酸根离子,其余三种离子转化为沉淀,过滤后再加盐酸,只发生沉淀与盐酸的反应,以此来解答.
解答:
解:加入过量的氢氧化钠溶液,微热并搅拌,四种离子均反应,铝离子转化为偏铝酸根离子,过滤后滤渣不含氢氧化铝,Al3+离子减小,
滤渣中含氢氧化镁、氢氧化亚铁、氢氧化铁,
即镁离子转化为沉淀后,再与盐酸反应生成镁离子,则Mg2+浓度不变,
亚铁离子转化为沉淀后被氧化生成氢氧化铁,与盐酸反应生成铁离子,则Fe2+浓度减小,Fe3+浓度增大,
故选BD.
滤渣中含氢氧化镁、氢氧化亚铁、氢氧化铁,
即镁离子转化为沉淀后,再与盐酸反应生成镁离子,则Mg2+浓度不变,
亚铁离子转化为沉淀后被氧化生成氢氧化铁,与盐酸反应生成铁离子,则Fe2+浓度减小,Fe3+浓度增大,
故选BD.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的考查,注意亚铁发生的氧化还原反应及滤渣中加盐酸,题目难度不大.

练习册系列答案
相关题目
食品添加剂让食品变得丰富多彩,但应正确使用食品添加剂.做馒头的过程中不能添加的是( )
| A、增白剂 | B、蔗糖 |
| C、小苏打 | D、食盐 |
化合物丙由如下反应制得:C4H
O
C4H
C4H
Br.丙的结构简式不可能的是( )
10 甲 |
| 浓硫酸,△ |
| 或Al2O4,△ |
8 乙 |
| Br2 |
| 溶液CCl4 |
8 丙 |
| A、CH3CH2CHBrCH2Br |
| B、CH3CH(CH2Br)2 |
| C、CH3CHBrCHBrCH3 |
| D、(CH3)2CBrCH2Br |
化学在生产和日常生活中有着重要的作用.下列有关说法不正确的是( )
| A、雾霾天气对人的健康造成危害,“雾”和“霾”的分散质微粒不相同 |
| B、氢氧化铁溶胶、蔗糖溶液、淀粉溶液均具有丁达尔效应 |
| C、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| D、只要符合限量,“食用色素”、“亚硝酸盐”可以作为某些食品的添加剂 |
下列说法正确的是( )
| A、碘是人体必需的微量元素,所以要多吃含I2的食盐 |
| B、半导体材料是含硅化合物 |
| C、熔化烧碱可选用瓷坩埚 |
| D、正长石KAlSi3O8用氧化物形式可表示为K2O?Al2O3?6SiO2 |
在室温下,某溶液中由水电离出的H+浓度为1.0×10-13 mol?L-1,则此溶液中一定能大量存在的离子组是( )
| A、Fe3+、NO3-、Cl-、Na+ |
| B、Ca2+、HCO3-、Cl-、K+ |
| C、NH4+、Fe2+、SO42-、NO3- |
| D、Cl-、SO42-、K+、Na+ |
 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用 kJ?mol-1表示.请认真观察下图,然后回答问题.
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用 kJ?mol-1表示.请认真观察下图,然后回答问题. 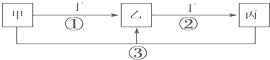 已知甲、乙、丙、丁是中学化学的常见物质,且甲、乙、丙均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).
已知甲、乙、丙、丁是中学化学的常见物质,且甲、乙、丙均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).