��Ŀ����
����Ŀ��Ϊ�˲ⶨij�л���A�Ľṹ��������ʵ�飺
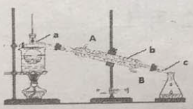
�ٽ�2.3g���л�����ȫȼ�գ�����0.1mol CO2��2.7gˮ��
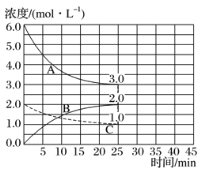
���������Dzⶨ����Է�������������ͼ(��)��ʾ������ͼ��
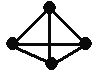
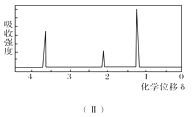
���ú˴Ź����Ǵ����û�����õ���ͼ(��)��ʾͼ�ף�ͼ������������֮����1��2��3��
�Իش��������⣺
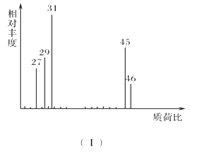
��1���л���A����Է���������________��
��2���л���A��ʵ��ʽ��________��
��3��A�ķ���ʽ��________��
��4���Ʋ��л���A�Ľṹ��ʽΪ____��A�к������ŵ�������_____��
���𰸡�46 C2H6O C2H6O CH3CH2OH �ǻ�
��������
��1�������ʺɱȿ�֪�����л���A����Է�����Ϊ46��
��2������2.3g���л�����ȼ�����ɵĶ�����̼��ˮ�����ж��л���A�е�̼Ԫ�ء���Ԫ�ص����ʵ��������������ж��Ƿ�����Ԫ�أ������C��H��OԪ�ص����ʵ���֮�ȣ����ȷ��A��ʵ��ʽ��
��3����Ϊʵ��ʽ��C2H6O���л����У���ԭ�����Ѿ��ﵽ���ͣ�������ʵ��ʽ��Ϊ����ʽ��
��4����Ϻ˴Ź��������жϸ��л�����ӵĽṹ��ʽ��
��1����A������ͼ�У�����ʺɱ�Ϊ46����������Է�������Ҳ��46���ʴ�Ϊ��46��
��2��2.3g���л����У�n(C)=n(CO2)=0.1mol�����е�̼ԭ�ӵ�����Ϊm(C)=0.1mol��12g��mol-1=1.2g����ԭ�ӵ����ʵ���Ϊ��n(H)=![]() ��2=0.3mol����ԭ�ӵ�����Ϊm(H)=0.3mol��1g��mol-1=0.3g�����л�����m(O)=2.3g-1.2g-0.3g=0.8g����Ԫ�ص����ʵ���Ϊn(O)=
��2=0.3mol����ԭ�ӵ�����Ϊm(H)=0.3mol��1g��mol-1=0.3g�����л�����m(O)=2.3g-1.2g-0.3g=0.8g����Ԫ�ص����ʵ���Ϊn(O)=![]() =0.05mol����n(C)��n(H)��n(O)=0.1mol��0.3mol��0.05mol=2��6��1������A��ʵ��ʽ�ǣ�C2H6O���ʴ�Ϊ��C2H6O��
=0.05mol����n(C)��n(H)��n(O)=0.1mol��0.3mol��0.05mol=2��6��1������A��ʵ��ʽ�ǣ�C2H6O���ʴ�Ϊ��C2H6O��
��3����Ϊʵ��ʽ��C2H6O���л����У���ԭ�����Ѿ��ﵽ���ͣ�������ʵ��ʽ��Ϊ����ʽ���ʴ�Ϊ��C2H6O��
��4��A���������ֿ��ܵĽṹ��CH3OCH3��CH3CH2OH����Ϊǰ�ߣ����ں˴Ź���������Ӧֻ��1���壻��Ϊ���ߣ����ں˴Ź���������Ӧ��3���壬����3��������֮����1��2��3����ȻCH3CH2OH�������⣬����AΪ�Ҵ����ṹ��ʽΪCH3CH2OH���Ҵ��Ĺ�����Ϊ�ǻ����ʴ�Ϊ��CH3CH2OH���ǻ���

 �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д� �������ͬ����ϰϵ�д�
�������ͬ����ϰϵ�д�