题目内容
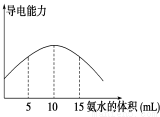
电离度是描述弱电解质电离程度的物理量,电离度=(已电离的电解质的物质的量/原来总的物质的量)×100%。现取20 mL pH=3 的 CH3COOH溶液,加入0.2 mol·L-1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为
A.0.5% B.1.5% C.0.1% D.1%
D
【解析】
试题分析:由图可知,加入氨水10mL时导电能力最强,说明此时氨水与醋酸恰好完全反应生成醋酸铵,所以醋酸溶液的物质的量浓度是0.2mol/L×10mL/20mL=0.1mol/L,即pH=3 的 CH3COOH溶液的浓度是0.1mol/L,c(H+)=10-3mol/L,所以加入氨水前CH3COOH的电离度=已电离的电解质的物质的量/原来总的物质的量)×100%=10-3mol/L/0.1mol/L×100%=1%,答案选D。
考点:考查弱电解质溶液电离度的计算

 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案(每空2分,共12分)
PCl3与PCl5均是有机合成的重要中间体,两者存在以下相互转化关系:
PCl5(g)  PCl3(g) + Cl2(g) △H=a kJ·mol-1 在210℃时,将4mol PCl5气体充入
PCl3(g) + Cl2(g) △H=a kJ·mol-1 在210℃时,将4mol PCl5气体充入
2L真空密闭容器中发生上述反应,得到如下数据:
时间(s) | 0 | 20 | 40 | 60 |
n(PCl5) | 4 | 2.8 | 2 | 2 |
(1)已知上述反应在温度较高时才能自发进行,则a 0(填﹥、﹦、﹤);
(2)计算从20s至40s共20s的时间内,用PCl3表示的平均反应速率为 。210℃时该反应的平衡常数K值等于 。
(3)反应进行至60s后,将混合物的温度降低,重新达到平衡后氯气浓度将 (填“增大”、“减少”或“不变”)。
(4)欲增大该反应的K值,可采取的措施有(填序号)
A.降低温度 B.向混合气体中通入Cl2
C.使用高效催化剂 D.升高温度
(5)如右图是210℃时容器中PCl5物质的量的变化曲线,请在该图中补画出该反应在160℃时PCl5物质的量的变化曲线。

 C(g)+D(g)发生过程中的能量变化如图,△H 表示反应的焓变。
C(g)+D(g)发生过程中的能量变化如图,△H 表示反应的焓变。