题目内容
4.氢氧燃料电池是一种高效、低污染的新型电池,主要用于航天领域.它的电极材料一般为活性电极,具有很强的催化活性,如铂电极、活性炭电极等.该电池氢气为燃料,氧气为氧化剂,可用酸性电解质(如稀H2SO4),也可用碱性电解质(如KOH).当用酸性电解质时,电极反应为:
正极:O2+2H2O+4e-=4OH-,
负极:2H2-4e-=4H+,
总反应:2H2+O2=2H2O.
当用碱性电解质时,电极反应式为:
正极:2H2-4e-+4OH-=4H2O,
负极:O2+2H2O+4e-=4OH-,
总反应:2H2+O2=2H2O.
分析 氢氧燃料电池工作时,负极发生氧化反应,正极发生还原反应,注意碱性电解质的条件下,负极产物是氢离子,正极产物是氢氧根离子,在酸性环境下,负极产物是氢离子,正极产物是水,总反应是氢气和氧气生成水的方程式.
解答 解:氢氧燃料电池工作时,氢气为燃料,负极燃料氢气发生氧化反应,正极是氧气发生还原反应,氧气是氧化剂,碱性氢氧燃料电池工作时,在负极上通入氢气,发生氧化反应,电极反应式为2H2-4e-+4OH-=4H2O,在正极上通入氧气,发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,
总反应为2H2+O2=2H2O,在酸性环境下,负极上通入氢气,发生氧化反应,电极反应式为2H2-4e-=4H+,在正极上通入氧气,发生还原反应,电极反应式为O2+4H++4e-=2H2O,总反应是氢气和氧气燃烧的方程式2H2+O2=2H2O,故答案为:氢气;氧气;酸、碱;KOH;O2+2H2O+4e-=4OH-;2H2-4e-=4H+;2H2+O2=2H2O;2H2-4e-+4OH-=4H2O;O2+2H2O+4e-=4OH-;2H2+O2=2H2O.
点评 本题考查原电池的工作原理知识,题目难度不大,注意电解质环境以及电极反应式的书写是关键.

练习册系列答案
相关题目
14.已知a、b分别为同周期的ⅠA和ⅥA族的两种元素,它们的原子序数分别为m和n,则下列关系不可能成立的是( )
| A. | n=m+15 | B. | n=m+5 | C. | n=m+29 | D. | n=m+9 |
15.下列说法正确的是( )
| A. | 氯气、硫酸钡和氨水分别属于非电解质、强电解质和弱电解质 | |
| B. | 体积不同但pH相同的醋酸和盐酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液的pH仍相同,而m和n无法确定相对大小 | |
| C. | CuCl2+2H2O?Cu(OH)2+2HCl,加入少量硝酸银固体后可以增大CuCl2水解程度 | |
| D. | 用来配制标准NaOH溶液的NaOH固体含有少量的KOH,此时中和测得盐酸的浓度数值一定偏高 |
12.在短周期元素中,原子最外电子层只有1个或2个电子的元素是( )
| A. | 一定是金属元素 | B. | 可能是稀有气体元素 | ||
| C. | 一定不是非金属元素 | D. | 原子容易失去电子的元素 |
9.在卤代烃RCH2CH2X中化学键如图,则对该卤代烃的下列说法中正确的是( )


| A. | 不能发生水解反应和消去反应 | |
| B. | 能发生水解反应,条件是强碱的醇溶液且加热,被破坏的键是①和④ | |
| C. | 能发生消去反应,条件是强碱的水溶液且加热,被破坏的键是①和② | |
| D. | 发生水解反应时,被破坏的键是①;发生消去反应时,被破坏的键是①和③ |
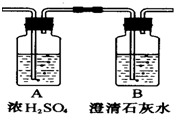 燃烧法是测定有机化合物化学式的一种重要方法.
燃烧法是测定有机化合物化学式的一种重要方法.
 .
. 按官能团分类的类别是酚.
按官能团分类的类别是酚. 按官能团分类的类别是酯.
按官能团分类的类别是酯.