题目内容
11.向l0mL1mol•L-1AlCl3溶液中加入l mol•L-1NaOH溶液生成沉淀0.26g.则所加NaOH的体积为( )| A. | 10 mL | B. | 20 mL | C. | 30 mL | D. | 36.7 mL |
分析 10mL mol/L的AlCl3溶液中氯化铝的物质的量=0.01L×mol/L=0.01mol,若Al元素都转化为氢氧化铝沉淀,则氢氧化铝沉淀的质量=0.01mol×78g/mol=0.78g>0.26g,说明有两种情况:一为沉淀不完全,只生成Al(OH)3沉淀;另一种情况为沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,结合方程式计算消耗氢氧化钠物质的量,进而计算需要氢氧化钠溶液体积.
解答 解:10mL mol/L的AlCl3溶液中氯化铝的物质的量=0.01L×mol/L=0.01mol,若Al元素都转化为氢氧化铝沉淀,则氢氧化铝沉淀的质量=0.01mol×78g/mol=0.78g>0.26g,说明有两种情况:一为沉淀不完全,只生成Al(OH)3沉淀;另一种情况为沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,
n(Al(OH)3)=$\frac{0.26g}{78g/mol}$=0.00333mol,
①若碱不足,由Al3++3OH-═Al(OH)3↓可知,
NaOH的物质的量为0.0033mol×3=0.00999mol,
加入NaOH溶液的体积为$\frac{0.00999mol}{1mol/L}$=0.00999L≈10mL;
②沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,则:
Al3++3OH-═Al(OH)3↓
0.01mol 0.03mol 0.01mol
Al(OH)3 +OH-═AlO2-+2H2O
(0.01-0.00333)mol (0.01-0.00333)mol
则消耗的碱的物质的量为0.03ol+(0.01-0.00333)mol=0.03667mol,
加入NaOH溶液的体积为$\frac{0.03667mol}{1mol/L}$=0.03667L≈36.7mL;
故选AD.
点评 本题考查方程式的有关计算,题目难度中等,关键是根据氯化铝与氢氧化铝的量判断发生的反应,再结合反应的有关方程式计算.

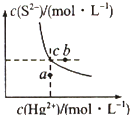 硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料、印泥及朱红雕刻漆器等.某温度时,HgS在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料、印泥及朱红雕刻漆器等.某温度时,HgS在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )| A. | 向硫化汞的浊液中加入硫化钠溶液,硫化汞的Ksp减小 | |
| B. | 图中a点对应的是饱和溶液 | |
| C. | 向c点的溶液中加入Hg(NO3)2,则c(S2-)减小 | |
| D. | 升高温度可以实现c点到b点的转化 |
| A. | 标准状况下,1mol任何物质的体积都约为22.4L | |
| B. | 1mol任何气体所含分子数都相同,体积也都约为22.4L | |
| C. | 同温同压下,相同体积的任何气体单质所含原子数目相同 | |
| D. | 常温常压下0.3mol H2、0.7mol N2组成的混合气体共含有NA个分子 |
| A. | 浓硝酸和稀硝酸都具有氧化性 | B. | 铜与硝酸的反应属于置换反应 | ||
| C. | 金属与硝酸反应不产生氢气 | D. | 可用铁或铝制品盛装浓硝酸 |
| A. | $\frac{a}{b{N}_{A}}$ | B. | $\frac{b}{a}$NA | C. | $\frac{a}{b}$ NA | D. | $\frac{b}{a{N}_{A}}$ |
| A. | MgCl2和H2O | B. | Mg(OH)2、HCl和H2O | C. | Mg、Cl2和H2O | D. | MgO、HCl和H2O |
| A. | 任何物质燃烧都必须有氧气参加 | |
| B. | 氢气在氯气中燃烧发出淡蓝色火焰,并在空气中产生大量白雾 | |
| C. | 饱和氯水在光照下有气泡产生,该气体为氯气 | |
| D. | 长久放置的氯水将失去漂白性 |
| A. | 任何晶体中,若含有阳离子也一定含有阴离子 | |
| B. | 原子晶体中只含有共价键 | |
| C. | 离子晶体中只含有离子键 | |
| D. | 分子晶体中只存在分子间作用力,不含化学键 |