题目内容
6.如果a g某气体中含有的分子数为b,则该气体在标准状况下的摩尔质量为( )| A. | $\frac{a}{b{N}_{A}}$ | B. | $\frac{b}{a}$NA | C. | $\frac{a}{b}$ NA | D. | $\frac{b}{a{N}_{A}}$ |
分析 先根据分子个数求出此气体的物质的量n,然后根据摩尔质量M=$\frac{m}{n}$来计算.
解答 解:a g某气体中含有的分子数为b,故其物质的量n=$\frac{b}{{N}_{A}}$mol,则摩尔质量M=$\frac{m}{n}$=$\frac{ag}{\frac{b}{{N}_{A}}mol}$=$\frac{a}{b}{N}_{A}$g/mol,故选C.
点评 本题考查了物质的摩尔质量的求算,应注意的是一种物质的摩尔质量与其所处的状态无关.

练习册系列答案
相关题目
12.关于如图各实验装置的叙述中,不正确的是( )

| A. | 利用图1装置可用于实验室制取少量NH3或O2 | |
| B. | 用图2可证明Cl2的氧化性强于S | |
| C. | 用图3所示装置可分离CH3CH2OH和CH3COOC2H5混合液 | |
| D. | 用图4所示装置可制取乙烯并验证其易被氧化 |
17.根据下列有关实验得出的结论一定正确的是( )
| 选项 | 方法 | 结论 |
| A | 同温时,等质量的锌粒分别与足量稀硫酸反应 | 产生氢气量:加过胆矾=没加胆矾 |
| B | 向Fe(NO3)2溶液中滴入用硫酸酸化的H2O2溶液,则溶液变黄 | 氧化性:H2O2>Fe3+ |
| C | 相同温度下,等质量的大理石与等体积、等浓度的盐酸反应 | 反应速率:粉状大理石>块状大理石 |
| D | 向2mL 0.1mol•L-1Na2S溶液中滴入几滴0.1mol•L-1ZnSO4溶液,有白色沉淀生成;再加入几滴0.1mol•L-1 CuSO4溶液,则又有黑色沉淀生成 | 溶度积(Ksp):ZnS>CuS |
| A. | A | B. | B | C. | C | D. | D |
1.填写下表:
| 物质的质量/g | 物质的量/mol | 微 粒/个 |
| 280g 铁原子 | 5 | 5NA |
| 3.4g氢氧根离子 | 0.2 | 0.2NA |
| 196 | 2mol硫酸分子 | 2NA |
| 19.2 | 0.8mol镁原子 | 0.8NA |
| 16 | 0.5 | 3.01×1023个氧分子 |
| 180 | 10 | 6.02×1024个铵根离子 |
11.向l0mL1mol•L-1AlCl3溶液中加入l mol•L-1NaOH溶液生成沉淀0.26g.则所加NaOH的体积为( )
| A. | 10 mL | B. | 20 mL | C. | 30 mL | D. | 36.7 mL |
18.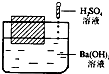 如图所示,在一只盛有Ba(OH)2溶液的烧杯中,漂浮着一个小木块,若小心地向烧杯中滴加与 Ba(OH)2溶液密度相同的稀硫酸,静止片刻后,小木块浸入液体中的体积与原先相比( )
如图所示,在一只盛有Ba(OH)2溶液的烧杯中,漂浮着一个小木块,若小心地向烧杯中滴加与 Ba(OH)2溶液密度相同的稀硫酸,静止片刻后,小木块浸入液体中的体积与原先相比( )
 如图所示,在一只盛有Ba(OH)2溶液的烧杯中,漂浮着一个小木块,若小心地向烧杯中滴加与 Ba(OH)2溶液密度相同的稀硫酸,静止片刻后,小木块浸入液体中的体积与原先相比( )
如图所示,在一只盛有Ba(OH)2溶液的烧杯中,漂浮着一个小木块,若小心地向烧杯中滴加与 Ba(OH)2溶液密度相同的稀硫酸,静止片刻后,小木块浸入液体中的体积与原先相比( )| A. | 增大 | B. | 不变 | C. | 减小 | D. | 无法判断 |
15.打雷及雷雨后,空气中的部分氮气最后转化成植物,能从土壤中吸收的是( )
| A. | N2 | B. | NO | C. | NH4+ | D. | 硝酸盐中的NO3- |