题目内容
(2011?南京一模)设nA为阿伏加德罗常数的值,下列叙述正确的是( )
分析:A、依据镁全部反应失去的电子计算;
B、一个 H3O+中含有电子为10个;
C、碳酸根离子水解生成两种阴离子,水存在电离平衡;
D、标准状况,水不是气体.
B、一个 H3O+中含有电子为10个;
C、碳酸根离子水解生成两种阴离子,水存在电离平衡;
D、标准状况,水不是气体.
解答:解:A、0.01mol Mg在空气中完全燃烧生成Mg0和Mg3N2.镁全部反应失电子总数是转移电子数,转移的电子数目为0.02nA,故AA正确;
B、1mol H3O+中含有的电子数目为10nA,故B错误;
C、100 mL l mol?L-1的Na2C03溶液中,碳酸根离子水解生成两种阴离子,含有的离子总数大于0.3nA,故C错误;
D、标准状况,水不是气体,44.8L H2O物质的量不是2mol,故D错误;
故选A.
B、1mol H3O+中含有的电子数目为10nA,故B错误;
C、100 mL l mol?L-1的Na2C03溶液中,碳酸根离子水解生成两种阴离子,含有的离子总数大于0.3nA,故C错误;
D、标准状况,水不是气体,44.8L H2O物质的量不是2mol,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的应用,主要是氧化还原反应电子转移数的计算,盐类水解的分析判断,气体摩尔体积的条件应用,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
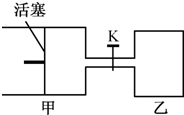 (2011?南京一模)如图所示,向甲和乙两容器中都充入2molX和2molY(K关闭) 起始V甲=0.8aL,V乙=aL,在相同恒定温度下,两容器中各自发生下列反应:X(g)+Y(g)═2Z(g)+W(g),达到平衡时,V甲=0.9aL,则下列说法错误的是( )
(2011?南京一模)如图所示,向甲和乙两容器中都充入2molX和2molY(K关闭) 起始V甲=0.8aL,V乙=aL,在相同恒定温度下,两容器中各自发生下列反应:X(g)+Y(g)═2Z(g)+W(g),达到平衡时,V甲=0.9aL,则下列说法错误的是( ) 是一种可限量使用的铁强化剂
是一种可限量使用的铁强化剂