题目内容
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
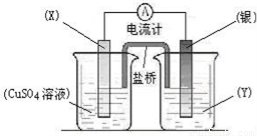
(1)电极X的材料是????????? (化学式);电解质溶液Y是??????????????????? ;
(2)银电极为电池的?????????? 极,发生的电极反应为?????????????????????? ;X电极上发生的电极反应为?????????????? ;
(3)外电路中的电子是从????? 电极流向?????? 电极。
【答案】
(10分)
(1)Cu (1分);AgNO3溶液 (2分)。
(2)正 (1分), Ag++e- = Ag (2分); Cu-2e- = Cu2+ (2分)。?
(3) 负(Cu) (1分);正(Ag) (1分)。
【解析】
试题分析:(1)由反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”可知,在反应中,Cu被氧化,失电子,应为原电池的负极,Ag+在正极上得电子被还原,电解质溶液为AgNO3 。
(2)正极为活泼性比Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,X电极为原电池的负极,Cu失去电子发生氧化还原反应: Cu-2e-=Cu2+。
(3)原电池中,电子从负极经外电路流向正极,本题中由Cu极经外电路流向Ag极。
考点:本题考查原电池的设计及工作原理、电极方程式的书写。

练习册系列答案
相关题目
 依据氧化还原反应:2Ag+ (aq)+Cu(s)═Cu2+ (aq)+2Ag(s)设计的原电池如图所示.
依据氧化还原反应:2Ag+ (aq)+Cu(s)═Cu2+ (aq)+2Ag(s)设计的原电池如图所示.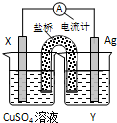 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题: 依据氧化还原反应:
依据氧化还原反应: