题目内容
18.下列操作或装置能达到实验目的是( )| A. | 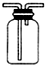 如图可用于收集气体H2、CO2、Cl2、NH3 | |
| B. | 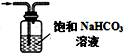 如图除去氯气中的氯化氢 | |
| C. | 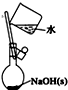 如图配制0.1mol/LNaOH溶液 | |
| D. |  如图苯萃取碘水中I2,分离出水后的操作 |
分析 A.H2、CO2、Cl2、NH3都可用排空气法收集,密度大小不同,可从不同的进气管进气
B.氯气和氯化氢都与碳酸氢钠反应;
C.不能在容量瓶中溶解氢氧化钠固体;
D.苯的密度小于水,应该从分液漏斗的上口倒出含碘单质的苯溶液.
解答 解:A.H2、NH3密度比空气小,从a进气,CO2、Cl2密度比空气大,从b进气,该装置可用于收集气体H2、CO2、Cl2、NH3,故A正确;
B.氯气能够与碳酸氢钠溶液反应,不能用饱和碳酸氢钠溶液除去氯气中的氯化氢,故B错误;
C.配制氢氧化钠溶液时,应该在烧杯中溶解氢氧化钠固体,不能直接用容量瓶溶解,故C错误;
D.苯萃取碘水中的碘,苯的密度小于水,在分液漏斗的上层,应从上口倒出,故D错误;
故选A.
点评 本题考查化学实验方案的评价,涉及物质分离与提纯、气体收集、溶液配制等知识,为高考常见题型,明确常见化学实验基本操作方法为解答关键,试题侧重于学生的分析能力和实验能力的考查.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列化合物中,含有离子键的是( )
| A. | CO2 | B. | HCl | C. | NH3 | D. | NaCl |
9.用惰性电极电解下列各溶液,经一段时间后,溶液的浓度增大,而溶液pH值保持不变的是( )
| A. | CuCl2溶液 | B. | KCl溶液 | C. | H2SO4溶液 | D. | K2SO4溶液 |
6.下列物质既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是( )
①Al2O3 ②Al(OH)3 ③Al.
①Al2O3 ②Al(OH)3 ③Al.
| A. | ①②③ | B. | ①和③ | C. | ②和③ | D. | ①和② |
7.下列有机反应属于同一反应类型的是( )
| A. | 乙烯使溴的四氯化碳溶液褪色;苯使溴水褪色 | |
| B. | 由苯制环己烷;乙酸制乙酸乙酯 | |
| C. | 苯制溴苯;由乙烯制乙醇 | |
| D. | 乙烯使酸性高锰酸钾溶液褪色;乙醇与灼热的氧化铜反应 |
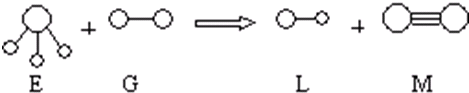
 .
.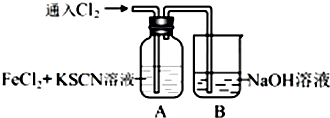
 ,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式为CN-+H2O2+H2O═NH3↑+HCO3-.
,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式为CN-+H2O2+H2O═NH3↑+HCO3-.