题目内容
6.漂白粉与酸作用放出的氯气称为有效氯,工业上常用有效氯与漂白粉质量的比值(x%)来表示漂白粉的优劣.反应原理:
Ca(ClO)Cl+H2SO4═CaSO4+Cl2+H2O
Cl2+2KI═2KCl+I2
2Na2S2O3+I2═Na2S4O6+2NaI
测定过程:称取某漂白精片0.2500g,加水研磨,小心地转入50mL容量瓶内,加水至刻度,摇匀,迅速吸取漂白粉悬浊液4.00mL,置于锥形瓶中,加入1.5mL3.0mol•L-1的H2SO4溶液和2mL10%KI溶液,加盖摇匀.在暗处放置5min后,加入几滴淀粉试液,用0.100mol•L-1的Na2S2O3标准溶液5.00mL滴定至蓝色刚好消失为止.
试由上述数据计算漂白粉的x%.88.75%.
分析 由反应方程式:Ca(ClO)Cl+H2SO4═CaSO4+Cl2+H2O、Cl2+2KI═2KCl+I2、2Na2S2O3+I2═Na2S4O6+2NaI可得,
关系式:Cl2~I2~2Na2S2O3,根据反应消耗的Na2S2O3的物质的量求出4.00mL漂白粉悬浊液中有效氯的物质的量,再求出50mL溶液中的有效氯,然后求出有效氯与漂白粉质量的比值.
解答 解:由反应方程式:Ca(ClO)Cl+H2SO4═CaSO4+Cl2+H2O、Cl2+2KI═2KCl+I2、2Na2S2O3+I2═Na2S4O6+2NaI可得,
关系式:Cl2~I2~2Na2S2O3,
1 2
n 0.100mol•L-1×5.00×10-3L
则n=2.5×10-4mol,
所以50mL溶液中的有效氯为 2.5×10-4mol×$\frac{50mL}{4mL}$×71g/mol=0.221875g,
则有效氯与漂白粉质量的比值为$\frac{0.221875g}{0.25g}$×100%=88.75%;
故答案为:88.75%.
点评 本题考查了有关化学方程式的计算、滴定原理的应用,题目难度中等,侧重于考查学生的分析能力和计算能力,注意根据已知反应方程式找出各物质之间的物质的量关系是解题的关键.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
17.某混合气体是由HF、(HF)2、(HF)3三种气体组成,该混合气体的平均相对分子质量为38,则混合气体中HF的体积分数为( )
| A. | 大于10% 小于55% | B. | 小于10% | C. | 等于10% | D. | 无法计算 |
14.下列关于物质的量浓度表述正确的是( )
| A. | 0.3 mol•L-1的Na2SO4溶液中含有Na+和SO42-的总物质的量为0.9 mol | |
| B. | 当1 L水吸收22.4 L HCl时所得的盐酸浓度不是1 mol/L,只有当22.4 L HCl溶于水制得1 L盐酸时,其浓度才是1 mol/L | |
| C. | 在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定相同 | |
| D. | 10℃时,100 mL 0.35 mol/L的KCl饱和溶液蒸发掉5 g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol/L |
18.能使水的电离平衡向右移动,且使溶液呈酸性的是( )
| A. | 向水中加入少量硫酸氢钠固体 | B. | 向水中加入少量硫酸铝固体 | ||
| C. | 向水中加入少量氯化铵固体 | D. | 将水加热到100℃,使水的pH=6 |
15.下列说法正确的是( )
| A. | 电镀铜时,电解质溶液中铜离子浓度不断减小 | |
| B. | 电解精炼铜时,电解质溶液中铜离子浓度不变 | |
| C. | 纯锌与稀硫酸反应时,加入少量CuSO4溶液,会使反应速率减慢 | |
| D. | 要使电解后的CuSO4溶液复原,可向其中加人CuO固体 |
16.氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既不是氧化剂又不是还原剂.下列反应与Cl2+SO2+2H2O=H2SO4+2HCl相比较,水的作用完全相同的是( )
| A. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | B. | 4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||
| C. | 2F2+2H2O=4HF+O2↑ | D. | 2Na+2H2O=2NaOH+H2↑ |
 ;试剂加入顺序是先加入浓硝酸,最后加入浓硫酸,该反应需要控制温度,方法是水浴加热.
;试剂加入顺序是先加入浓硝酸,最后加入浓硫酸,该反应需要控制温度,方法是水浴加热.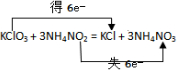 .
.