题目内容
17.某混合气体是由HF、(HF)2、(HF)3三种气体组成,该混合气体的平均相对分子质量为38,则混合气体中HF的体积分数为( )| A. | 大于10% 小于55% | B. | 小于10% | C. | 等于10% | D. | 无法计算 |
分析 根据HF、(HF)2、(HF)3的摩尔质量判断混合气体的可能组成情况,然后利用极值法判断混合气体中氟化氢的体积分数范围,再根据计算结果进行判断.
解答 解:HF、(HF)2、(HF)3的摩尔质量分别为20g/mol,40g/mol、60g/mol,混合气体的平均相对分子质量为38,即摩尔质量为38g/mol,则混合气体中一定含有HF,可能为HF和(HF)2、HF和(HF)3或HF、(HF)2、(HF)3三种情况:
根据极限假设法:当混合气体为HF和(HF)2时,设氟化氢HF的体积为x,(HF)2的体积为y,则:$\frac{20x+40y}{x+y}$=38,解得:x:y=1:9,所以HF的体积分数为:$\frac{1}{1+9}$×100%=10%;
当混合气体为HF和(HF)3时,设HF的体积为x,(HF)3的体积为y,则:$\frac{20x+60y}{x+y}$=38,解得:x:y=11:9,HF的体积分数为:$\frac{11}{11+9}$×100%=55%,
所以混合气体中氟化氢的体积分数介于10%~55%之间,
故选A.
点评 本题主要考查了有关混合物的计算,题目难度不大,注意极值法的应用,正确判断混合气体的可能组成为解答本题的关键,培养了学生分析、理解能力及化学计算能力.

练习册系列答案
相关题目
7.除去下列物质中的少量杂质(括号内的物质为杂质),所选出的试剂或方法不正确的是( )
| A. | CO2(SO2):饱和碳酸氢钠溶液 | B. | N2(O2):灼热的铜网 | ||
| C. | Al2O3(SiO2):NaOH溶液 | D. | Na2CO3固体(NaHCO3):加热 |
2.如图下列仪器,可以直接加热的是( )
| A. | 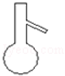 | B. |  | C. |  | D. |  |
9.“促进低碳经济”是世界环境日的主题,《联合国气候变化框架公约》第15次缔约方会议也商讨了2012年至2020年的全球减排协议.下列行为中不符合“促进低碳经济”宗旨的是( )
| A. | 开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料 | |
| B. | 将煤进行气化处理,提高煤的综合利用效率 | |
| C. | 研究采煤、采油新技术,提高产量以满足工业生产的快速发展 | |
| D. | 实现资源的“3R”利用观,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle) |
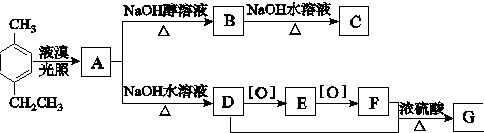
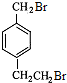 .
.
 .
.