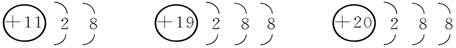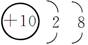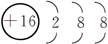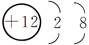题目内容
现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4②1s22s22p63s23p3③1s22s22p3④1s22s22p5
则下列有关比较中正确的是( )
| A.第一电离能:④>③>②>① |
| B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① |
| D.最高正化合价:④>③=②>① |
A
解析

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
X2-的核外电子排布为2、8、8,则X元素在周期表中的位置是
| A.第三周期0族 | B.第三周期VIA族 |
| C.第三周期VIIA族 | D.第四周期IA族 |
Mg、Ca、Sr、Ba是按原子序数由小到大的顺序排列的第ⅡA族元素。已知:①Mg(OH)2难溶于水,而Ca(OH)2微溶于水;②MgSO4溶于水,而CaSO4微溶于水。下列推测中,不正确的是( )。
| A.Sr(OH)2溶解于水 | B.SrSO4易溶于水 |
| C.BaSO4不溶于水 | D.Ba(OH)2比Ca(OH)2更易溶于水 |
元素的种类和原子的种类( )。
| A.前者多 | B.后者多 | C.相同 | D.无法确定 |
下列叙述中正确的是( )
| A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子 |
| B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子 |
| C.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高 |
| D.如果某一基态原子3p能级上仅有2个电子,它们的自旋方向必然相反 |
某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述中错误的是( )
| A.它是副族元素 |
| B.它是第六周期元素 |
| C.它的原子核内有63个质子 |
| D.它的一种同位素的核内有89个中子 |